Ольга «Если его умножить на 4, к произведению прибавить 8 и полученную сумму разделить
на 2, то получится 10». Обозначим за x число. Умножим на 4 ; 4x. Прибавим 8 ; 4x + 8.
Полученную сумму поделим на 2; (4x + 8)/2. И все это теперь равно 10 ; (4x + 8)/2 = 10
Задание
Развернуть задание
Вычислить объем водорода (н.у.), который может быть получен при растворении в едком натре 270 мг сплава, содержащего 5% меди. Выход водорода принять равным 85% от теоретически возможного.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
1. ω(Al) = 100% - ω(Cu) = 100% - 5% = 95% или 0,95
2. m(Al) = m(сплава) ∙ ω(Al) = 0,27 ∙ 0,95 = 0,257 г
3. Составим соотношение и найдем теоретический объем водорода:
2. m(Al) = m(сплава) ∙ ω(Al) = 0,27 ∙ 0,95 = 0,257 г
3. Составим соотношение и найдем теоретический объем водорода:
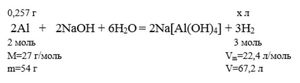
из 54 г алюминия образуется 67,2 л водорода
из 0,257 г алюминия образуется x л водорода
Vтеор(H2) = x = 0,257 ∙ 67,2 / 54 = 0,3198 л
4. Vпр (H2) = Vтеор(H2) ∙ η = 0,3198 ∙ 0,85 = 0,2718 л = 271,8 мл
Ответ: Vпр(H2) = 271,8 мл.
из 0,257 г алюминия образуется x л водорода
Vтеор(H2) = x = 0,257 ∙ 67,2 / 54 = 0,3198 л
4. Vпр (H2) = Vтеор(H2) ∙ η = 0,3198 ∙ 0,85 = 0,2718 л = 271,8 мл
Ответ: Vпр(H2) = 271,8 мл.
1. ω(Al) = 100% - ω(Cu) = 100% - 5% = 95% или 0,95
2. m(Al) = m(сплава) ∙ ω(Al) = 0,27 ∙ 0,95 = 0,257 г
3. Составим соотношение и найдем теоретический объем водорода:
2. m(Al) = m(сплава) ∙ ω(Al) = 0,27 ∙ 0,95 = 0,257 г
3. Составим соотношение и найдем теоретический объем водорода:
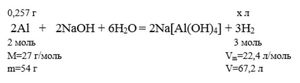
из 54 г алюминия образуется 67,2 л водорода
из 0,257 г алюминия образуется x л водорода
Vтеор(H2) = x = 0,257 ∙ 67,2 / 54 = 0,3198 л
4. Vпр (H2) = Vтеор(H2) ∙ η = 0,3198 ∙ 0,85 = 0,2718 л = 271,8 мл
Ответ: Vпр(H2) = 271,8 мл.
из 0,257 г алюминия образуется x л водорода
Vтеор(H2) = x = 0,257 ∙ 67,2 / 54 = 0,3198 л
4. Vпр (H2) = Vтеор(H2) ∙ η = 0,3198 ∙ 0,85 = 0,2718 л = 271,8 мл
Ответ: Vпр(H2) = 271,8 мл.