Задание
Развернуть задание
Вычислить объем оксида углерода (II) (н.у.), который потребуется для восстановления железа из 2,32 т магнитного железняка, содержащего 5% пустой породы. Вычислить количество вещества железа, которое при этом получится, если выход его составляет 80% от теоретически возможного.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
Решение:
1. ω(Fe3O4) = 100% - ω(Fe3O4) = 100% - 5% = 95% или 0,95
2. m(Fe3O4) = m(т. Fe3O4) ∙ ω(Fe3O4) = 2,32 ∙ 0,95 = 2,204 т = 2,204∙106 г
3. Составим уравнение реакции восстановления железа из магнитного железняка Fe3O4:
1. ω(Fe3O4) = 100% - ω(Fe3O4) = 100% - 5% = 95% или 0,95
2. m(Fe3O4) = m(т. Fe3O4) ∙ ω(Fe3O4) = 2,32 ∙ 0,95 = 2,204 т = 2,204∙106 г
3. Составим уравнение реакции восстановления железа из магнитного железняка Fe3O4:
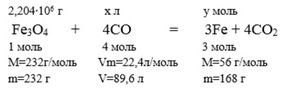
4. Найдем V(CO) и m(Fe):
на восстановление 232 г Fe3O4 требуется 89,6 л СО
на восстановление 2,204∙106 г Fe3O4 требуется x л СО
V(CO) = x = 2,204∙106 ∙ 89,6 / 232 = 8,521∙105 л
из 232 г Fe3O4 образуется 168 г Fe
из 2,204∙106 г Fe3O4 образуется y г Fe
m(Fe) = y = 2,204∙106 ∙ 168 / 232 = 1,596∙106 г
5. Рассчитаем количество вещества железа, которое должно было получиться в ходе реакции:
M(Fe) = 56 г/моль
n(Fe) = m / M = 1,596∙106 / 56 = 2,85∙104 моль
6. Рассчитаем количество вещества железа, которое получилось на практике:
n_пр (Fe) = nтеор(Fe) ∙ η = 2,85∙104 ∙ 0,8 = 2,28∙104 моль
Ответ: V(СО) = 8,512 ∙ 105 л, n_пр (Fe) = 2,28∙104 моль
на восстановление 232 г Fe3O4 требуется 89,6 л СО
на восстановление 2,204∙106 г Fe3O4 требуется x л СО
V(CO) = x = 2,204∙106 ∙ 89,6 / 232 = 8,521∙105 л
из 232 г Fe3O4 образуется 168 г Fe
из 2,204∙106 г Fe3O4 образуется y г Fe
m(Fe) = y = 2,204∙106 ∙ 168 / 232 = 1,596∙106 г
5. Рассчитаем количество вещества железа, которое должно было получиться в ходе реакции:
M(Fe) = 56 г/моль
n(Fe) = m / M = 1,596∙106 / 56 = 2,85∙104 моль
6. Рассчитаем количество вещества железа, которое получилось на практике:
n_пр (Fe) = nтеор(Fe) ∙ η = 2,85∙104 ∙ 0,8 = 2,28∙104 моль
Ответ: V(СО) = 8,512 ∙ 105 л, n_пр (Fe) = 2,28∙104 моль
Решение:
1. ω(Fe3O4) = 100% - ω(Fe3O4) = 100% - 5% = 95% или 0,95
2. m(Fe3O4) = m(т. Fe3O4) ∙ ω(Fe3O4) = 2,32 ∙ 0,95 = 2,204 т = 2,204∙106 г
3. Составим уравнение реакции восстановления железа из магнитного железняка Fe3O4:
1. ω(Fe3O4) = 100% - ω(Fe3O4) = 100% - 5% = 95% или 0,95
2. m(Fe3O4) = m(т. Fe3O4) ∙ ω(Fe3O4) = 2,32 ∙ 0,95 = 2,204 т = 2,204∙106 г
3. Составим уравнение реакции восстановления железа из магнитного железняка Fe3O4:
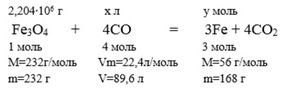
4. Найдем V(CO) и m(Fe):
на восстановление 232 г Fe3O4 требуется 89,6 л СО
на восстановление 2,204∙106 г Fe3O4 требуется x л СО
V(CO) = x = 2,204∙106 ∙ 89,6 / 232 = 8,521∙105 л
из 232 г Fe3O4 образуется 168 г Fe
из 2,204∙106 г Fe3O4 образуется y г Fe
m(Fe) = y = 2,204∙106 ∙ 168 / 232 = 1,596∙106 г
5. Рассчитаем количество вещества железа, которое должно было получиться в ходе реакции:
M(Fe) = 56 г/моль
n(Fe) = m / M = 1,596∙106 / 56 = 2,85∙104 моль
6. Рассчитаем количество вещества железа, которое получилось на практике:
n_пр (Fe) = nтеор(Fe) ∙ η = 2,85∙104 ∙ 0,8 = 2,28∙104 моль
Ответ: V(СО) = 8,512 ∙ 105 л, n_пр (Fe) = 2,28∙104 моль
на восстановление 232 г Fe3O4 требуется 89,6 л СО
на восстановление 2,204∙106 г Fe3O4 требуется x л СО
V(CO) = x = 2,204∙106 ∙ 89,6 / 232 = 8,521∙105 л
из 232 г Fe3O4 образуется 168 г Fe
из 2,204∙106 г Fe3O4 образуется y г Fe
m(Fe) = y = 2,204∙106 ∙ 168 / 232 = 1,596∙106 г
5. Рассчитаем количество вещества железа, которое должно было получиться в ходе реакции:
M(Fe) = 56 г/моль
n(Fe) = m / M = 1,596∙106 / 56 = 2,85∙104 моль
6. Рассчитаем количество вещества железа, которое получилось на практике:
n_пр (Fe) = nтеор(Fe) ∙ η = 2,85∙104 ∙ 0,8 = 2,28∙104 моль
Ответ: V(СО) = 8,512 ∙ 105 л, n_пр (Fe) = 2,28∙104 моль