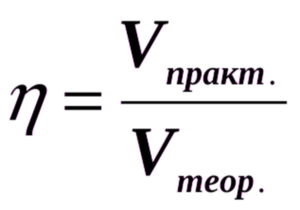Задание
Развернуть задание
Рассчитайте объём ацетилена, который может быть получен из 128 г карбида кальция, содержащего 5 % примесей, если выход ацетилена составляет 80% от теоретически возможного.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
Дано:
На практике ацетилен часто получают из карбида кальция:
CaC 2 +2HOH C 2 H 2 +Ca(OH) 2
m(CaC 2 +примеси)=128 г
ω(примесей в CaC 2 )=5%
η выхода (C 2 H 2 )=80%=0,8
V(C 2 H 2 )=?
Решение:
1) Найдём примеси в карбиде кальция из формулы картинка №1:
m(примесей)=5%*128 г/100%=6,4 г
m(чистого CaC2 )=128 г – 6,4 г=121,6 г
2) Составим пропорцию для вычисления теоретического объёма ацетилена = х:
64 г СаС2 – 22,4 л С2Н2
121,6 г СаС2 – х л С2Н2
Х=121,6 г*22,4 л/64 г=42,56 л
3) Зная формулу (картинка №2) , можем рассчитать практический объём ацетилена:
V практический (С 2 Н 2 )=0,8*42,56 л=34,05 л
Ответ: V практический (С 2 Н 2 )=0,8*42,56 л=34,05 л
На практике ацетилен часто получают из карбида кальция:
CaC 2 +2HOH C 2 H 2 +Ca(OH) 2
m(CaC 2 +примеси)=128 г
ω(примесей в CaC 2 )=5%
η выхода (C 2 H 2 )=80%=0,8
V(C 2 H 2 )=?
Решение:
1) Найдём примеси в карбиде кальция из формулы картинка №1:
m(примесей)=5%*128 г/100%=6,4 г
m(чистого CaC2 )=128 г – 6,4 г=121,6 г
2) Составим пропорцию для вычисления теоретического объёма ацетилена = х:
64 г СаС2 – 22,4 л С2Н2
121,6 г СаС2 – х л С2Н2
Х=121,6 г*22,4 л/64 г=42,56 л
3) Зная формулу (картинка №2) , можем рассчитать практический объём ацетилена:
V практический (С 2 Н 2 )=0,8*42,56 л=34,05 л
Ответ: V практический (С 2 Н 2 )=0,8*42,56 л=34,05 л

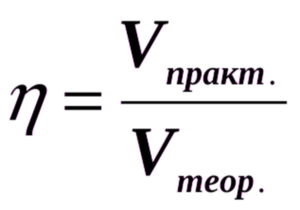
Дано:
На практике ацетилен часто получают из карбида кальция:
CaC 2 +2HOH C 2 H 2 +Ca(OH) 2
m(CaC 2 +примеси)=128 г
ω(примесей в CaC 2 )=5%
η выхода (C 2 H 2 )=80%=0,8
V(C 2 H 2 )=?
Решение:
1) Найдём примеси в карбиде кальция из формулы картинка №1:
m(примесей)=5%*128 г/100%=6,4 г
m(чистого CaC2 )=128 г – 6,4 г=121,6 г
2) Составим пропорцию для вычисления теоретического объёма ацетилена = х:
64 г СаС2 – 22,4 л С2Н2
121,6 г СаС2 – х л С2Н2
Х=121,6 г*22,4 л/64 г=42,56 л
3) Зная формулу (картинка №2) , можем рассчитать практический объём ацетилена:
V практический (С 2 Н 2 )=0,8*42,56 л=34,05 л
Ответ: V практический (С 2 Н 2 )=0,8*42,56 л=34,05 л
На практике ацетилен часто получают из карбида кальция:
CaC 2 +2HOH C 2 H 2 +Ca(OH) 2
m(CaC 2 +примеси)=128 г
ω(примесей в CaC 2 )=5%
η выхода (C 2 H 2 )=80%=0,8
V(C 2 H 2 )=?
Решение:
1) Найдём примеси в карбиде кальция из формулы картинка №1:
m(примесей)=5%*128 г/100%=6,4 г
m(чистого CaC2 )=128 г – 6,4 г=121,6 г
2) Составим пропорцию для вычисления теоретического объёма ацетилена = х:
64 г СаС2 – 22,4 л С2Н2
121,6 г СаС2 – х л С2Н2
Х=121,6 г*22,4 л/64 г=42,56 л
3) Зная формулу (картинка №2) , можем рассчитать практический объём ацетилена:
V практический (С 2 Н 2 )=0,8*42,56 л=34,05 л
Ответ: V практический (С 2 Н 2 )=0,8*42,56 л=34,05 л