Ира М(С4Н10) = 4*12 + 10*1 = 58 г/моль
ω(C) = 4*12 / 58*100% = 82,8%
М(С5Н12) = 5*12 + 12*1 = 72 г/моль
ω (C) = 5*12 / 72*100% = 83,3%
Задание
Развернуть задание
Вычислить объем водорода (н.у.), который образуется при растворении 100 г латуни, содержащей 13% цинка, в соляной кислоте.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
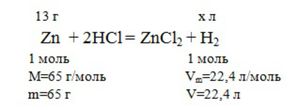
Из уравнения следует, что для получения H2 объемом 22,4 л требуется 65 г цинка.
из 65 г Zn образуется 22,4 л H2
из 13 г Zn образуется x л H2
x = 13 ∙ 22,4 / 65 = 4,48 л
Ответ: 4,48 л.
из 65 г Zn образуется 22,4 л H2
из 13 г Zn образуется x л H2
x = 13 ∙ 22,4 / 65 = 4,48 л
Ответ: 4,48 л.
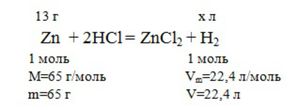
Из уравнения следует, что для получения H2 объемом 22,4 л требуется 65 г цинка.
из 65 г Zn образуется 22,4 л H2
из 13 г Zn образуется x л H2
x = 13 ∙ 22,4 / 65 = 4,48 л
Ответ: 4,48 л.
из 65 г Zn образуется 22,4 л H2
из 13 г Zn образуется x л H2
x = 13 ∙ 22,4 / 65 = 4,48 л
Ответ: 4,48 л.