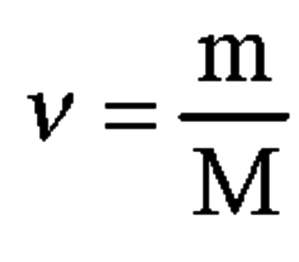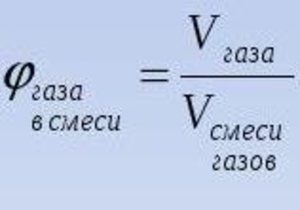Задание
Развернуть задание
Вычислить объем воздуха (н.у.), который потребуется для сжигания 36 г магния.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
Дано:
m(Mg) = 36 г
φ(O(2)) = 0,21
V(воздуха) - ?
Решение:
1. Составим уравнение реакции сжигания магния:
1,5 моль x моль
2Mg + O 2 = 2MgO
2 моль 1 моль
2. Вычислим количество вещества магния Mg по формуле, представленной на 1 картинке.
M(Mg) = 24 г/моль
n(Mg) = 36 / 24 = 1,5 моль
3. По уравнению реакции с 2 моль магния реагирует 1 моль кислорода. Тогда, для окисления 1,5 моль магния надо в 2 раза меньшее количество кислорода:
n(O(2)) = 1,5 ∙ 1 / 2 = 0,75 моль
4. Так как условия нормальные можно вычислить объем O(2) используя мольный объем:
V(O(2)) = n(O(2)) ∙ V(m)=0,75 ∙ 22,4 = 16,8 л.
5. Определим объем воздуха, необходимый для сжигания 36 г магния. Так как в воздухе содержится 21 % кислорода, то можно воспользоваться формулой, представленной на 2 картинке.
V(возд.) = V(O(2)) / φ(O(2)) = 16,8 / 0,21 = 80 л.
Ответ: V(возд.) = 80 л.
m(Mg) = 36 г
φ(O(2)) = 0,21
V(воздуха) - ?
Решение:
1. Составим уравнение реакции сжигания магния:
1,5 моль x моль
2Mg + O 2 = 2MgO
2 моль 1 моль
2. Вычислим количество вещества магния Mg по формуле, представленной на 1 картинке.
M(Mg) = 24 г/моль
n(Mg) = 36 / 24 = 1,5 моль
3. По уравнению реакции с 2 моль магния реагирует 1 моль кислорода. Тогда, для окисления 1,5 моль магния надо в 2 раза меньшее количество кислорода:
n(O(2)) = 1,5 ∙ 1 / 2 = 0,75 моль
4. Так как условия нормальные можно вычислить объем O(2) используя мольный объем:
V(O(2)) = n(O(2)) ∙ V(m)=0,75 ∙ 22,4 = 16,8 л.
5. Определим объем воздуха, необходимый для сжигания 36 г магния. Так как в воздухе содержится 21 % кислорода, то можно воспользоваться формулой, представленной на 2 картинке.
V(возд.) = V(O(2)) / φ(O(2)) = 16,8 / 0,21 = 80 л.
Ответ: V(возд.) = 80 л.
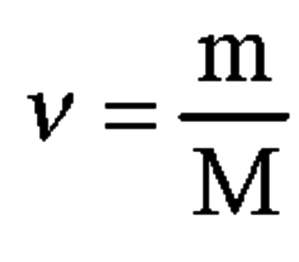
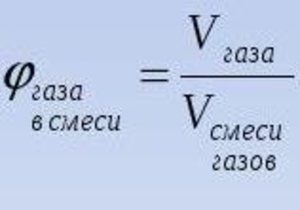
Дано:
m(Mg) = 36 г
φ(O(2)) = 0,21
V(воздуха) - ?
Решение:
1. Составим уравнение реакции сжигания магния:
1,5 моль x моль
2Mg + O 2 = 2MgO
2 моль 1 моль
2. Вычислим количество вещества магния Mg по формуле, представленной на 1 картинке.
M(Mg) = 24 г/моль
n(Mg) = 36 / 24 = 1,5 моль
3. По уравнению реакции с 2 моль магния реагирует 1 моль кислорода. Тогда, для окисления 1,5 моль магния надо в 2 раза меньшее количество кислорода:
n(O(2)) = 1,5 ∙ 1 / 2 = 0,75 моль
4. Так как условия нормальные можно вычислить объем O(2) используя мольный объем:
V(O(2)) = n(O(2)) ∙ V(m)=0,75 ∙ 22,4 = 16,8 л.
5. Определим объем воздуха, необходимый для сжигания 36 г магния. Так как в воздухе содержится 21 % кислорода, то можно воспользоваться формулой, представленной на 2 картинке.
V(возд.) = V(O(2)) / φ(O(2)) = 16,8 / 0,21 = 80 л.
Ответ: V(возд.) = 80 л.
m(Mg) = 36 г
φ(O(2)) = 0,21
V(воздуха) - ?
Решение:
1. Составим уравнение реакции сжигания магния:
1,5 моль x моль
2Mg + O 2 = 2MgO
2 моль 1 моль
2. Вычислим количество вещества магния Mg по формуле, представленной на 1 картинке.
M(Mg) = 24 г/моль
n(Mg) = 36 / 24 = 1,5 моль
3. По уравнению реакции с 2 моль магния реагирует 1 моль кислорода. Тогда, для окисления 1,5 моль магния надо в 2 раза меньшее количество кислорода:
n(O(2)) = 1,5 ∙ 1 / 2 = 0,75 моль
4. Так как условия нормальные можно вычислить объем O(2) используя мольный объем:
V(O(2)) = n(O(2)) ∙ V(m)=0,75 ∙ 22,4 = 16,8 л.
5. Определим объем воздуха, необходимый для сжигания 36 г магния. Так как в воздухе содержится 21 % кислорода, то можно воспользоваться формулой, представленной на 2 картинке.
V(возд.) = V(O(2)) / φ(O(2)) = 16,8 / 0,21 = 80 л.
Ответ: V(возд.) = 80 л.