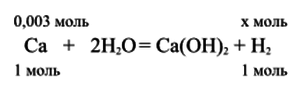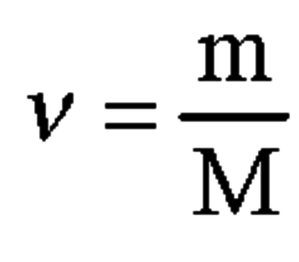Задание
Развернуть задание
Вычислить объем водорода (н.у.), который может быть получен при растворении в воде 120 мг кальция, если выход газа составляет 80 % от теоретически возможного.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
Дано:
m(Ca) = 120 мг = 0,12 г
η(H(2)) = 80 % или 0,8
Vпр (H(2)) - ?
Решение:
1. Составим уравнение реакции: 1 картинка
2. Вычислим количество вещества Ca по формуле, представленной на 2 картинке:
M(Ca) = 40 г/моль
n(Mg) = 0,12 / 40 = 0,003 моль
3. Вычислим теоретическое n(теор)(H(2)). По уравнению реакции из 1 моль кальция образуется 1 моль водорода, тогда из 0,003 моль кальция образуется равное количество водорода:
n(H(2))теор = n(Ca) = 0,003 моль
4. Вычислим объем H(2), который теоретически должен был получиться в ходе протекания реакции. Так как условия нормальные, можно использовать мольный объем:
Vтеор (H(2)) = n(теор)(H(2)) ∙ V(m) = 0,003 ∙ 22,4 = 0,0672 л
5. Определим практический объем водорода, используя формулу, представленную на 3 картинке:
Vпракт(H(2)) = Vтеор(H() ) ∙ η(H(2)) = 0,0672 ∙ 0,8 = 0,05376 л = 53,76 мл
Ответ: V практ (H 2 ) = 53,76 мл.
m(Ca) = 120 мг = 0,12 г
η(H(2)) = 80 % или 0,8
Vпр (H(2)) - ?
Решение:
1. Составим уравнение реакции: 1 картинка
2. Вычислим количество вещества Ca по формуле, представленной на 2 картинке:
M(Ca) = 40 г/моль
n(Mg) = 0,12 / 40 = 0,003 моль
3. Вычислим теоретическое n(теор)(H(2)). По уравнению реакции из 1 моль кальция образуется 1 моль водорода, тогда из 0,003 моль кальция образуется равное количество водорода:
n(H(2))теор = n(Ca) = 0,003 моль
4. Вычислим объем H(2), который теоретически должен был получиться в ходе протекания реакции. Так как условия нормальные, можно использовать мольный объем:
Vтеор (H(2)) = n(теор)(H(2)) ∙ V(m) = 0,003 ∙ 22,4 = 0,0672 л
5. Определим практический объем водорода, используя формулу, представленную на 3 картинке:
Vпракт(H(2)) = Vтеор(H() ) ∙ η(H(2)) = 0,0672 ∙ 0,8 = 0,05376 л = 53,76 мл
Ответ: V практ (H 2 ) = 53,76 мл.
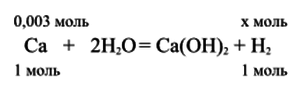
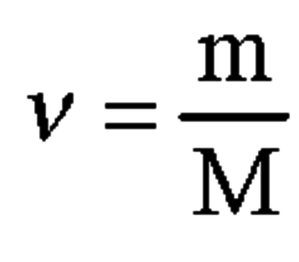

Дано:
m(Ca) = 120 мг = 0,12 г
η(H(2)) = 80 % или 0,8
Vпр (H(2)) - ?
Решение:
1. Составим уравнение реакции: 1 картинка
2. Вычислим количество вещества Ca по формуле, представленной на 2 картинке:
M(Ca) = 40 г/моль
n(Mg) = 0,12 / 40 = 0,003 моль
3. Вычислим теоретическое n(теор)(H(2)). По уравнению реакции из 1 моль кальция образуется 1 моль водорода, тогда из 0,003 моль кальция образуется равное количество водорода:
n(H(2))теор = n(Ca) = 0,003 моль
4. Вычислим объем H(2), который теоретически должен был получиться в ходе протекания реакции. Так как условия нормальные, можно использовать мольный объем:
Vтеор (H(2)) = n(теор)(H(2)) ∙ V(m) = 0,003 ∙ 22,4 = 0,0672 л
5. Определим практический объем водорода, используя формулу, представленную на 3 картинке:
Vпракт(H(2)) = Vтеор(H() ) ∙ η(H(2)) = 0,0672 ∙ 0,8 = 0,05376 л = 53,76 мл
Ответ: V практ (H 2 ) = 53,76 мл.
m(Ca) = 120 мг = 0,12 г
η(H(2)) = 80 % или 0,8
Vпр (H(2)) - ?
Решение:
1. Составим уравнение реакции: 1 картинка
2. Вычислим количество вещества Ca по формуле, представленной на 2 картинке:
M(Ca) = 40 г/моль
n(Mg) = 0,12 / 40 = 0,003 моль
3. Вычислим теоретическое n(теор)(H(2)). По уравнению реакции из 1 моль кальция образуется 1 моль водорода, тогда из 0,003 моль кальция образуется равное количество водорода:
n(H(2))теор = n(Ca) = 0,003 моль
4. Вычислим объем H(2), который теоретически должен был получиться в ходе протекания реакции. Так как условия нормальные, можно использовать мольный объем:
Vтеор (H(2)) = n(теор)(H(2)) ∙ V(m) = 0,003 ∙ 22,4 = 0,0672 л
5. Определим практический объем водорода, используя формулу, представленную на 3 картинке:
Vпракт(H(2)) = Vтеор(H() ) ∙ η(H(2)) = 0,0672 ∙ 0,8 = 0,05376 л = 53,76 мл
Ответ: V практ (H 2 ) = 53,76 мл.