Задание
Развернуть задание
Вычислить объем водорода (н.у.), который может быть получен при растворении в воде 11,5 г натрия, содержащего 2% примесей, если выход водорода составляет 95% от теоретически возможного.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
1. Рассчитаем массовую долю чистого натрия в смеси:
ω(Na) = 100% - ω(прим.) = 100% - 2% = 98% или 0,98
2. Найдем массу чистого натрия:
m(Na) = m(т.Na) ∙ ω(Na) = 11,5 ∙ 0,98 = 11,27 г
3. Составим уравнение реакции и найдем объем водорода, который теоретически должен был получиться в ходе реакции:
ω(Na) = 100% - ω(прим.) = 100% - 2% = 98% или 0,98
2. Найдем массу чистого натрия:
m(Na) = m(т.Na) ∙ ω(Na) = 11,5 ∙ 0,98 = 11,27 г
3. Составим уравнение реакции и найдем объем водорода, который теоретически должен был получиться в ходе реакции:
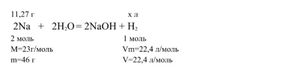
46 г Na образует 22,4 л/моль
11,27 г Na образует x л
Vтеор (H2) = х = 11,27 ∙ 22,4 / 46 = 5,488 л
4. Определим объем водорода, который был получен практически.
Vпр (H2) = Vтеор (H2) ∙ η = 5,488 ∙ 0,95 = 5,2136 л
Ответ: V(H2) = 5,2136 л.
11,27 г Na образует x л
Vтеор (H2) = х = 11,27 ∙ 22,4 / 46 = 5,488 л
4. Определим объем водорода, который был получен практически.
Vпр (H2) = Vтеор (H2) ∙ η = 5,488 ∙ 0,95 = 5,2136 л
Ответ: V(H2) = 5,2136 л.
1. Рассчитаем массовую долю чистого натрия в смеси:
ω(Na) = 100% - ω(прим.) = 100% - 2% = 98% или 0,98
2. Найдем массу чистого натрия:
m(Na) = m(т.Na) ∙ ω(Na) = 11,5 ∙ 0,98 = 11,27 г
3. Составим уравнение реакции и найдем объем водорода, который теоретически должен был получиться в ходе реакции:
ω(Na) = 100% - ω(прим.) = 100% - 2% = 98% или 0,98
2. Найдем массу чистого натрия:
m(Na) = m(т.Na) ∙ ω(Na) = 11,5 ∙ 0,98 = 11,27 г
3. Составим уравнение реакции и найдем объем водорода, который теоретически должен был получиться в ходе реакции:
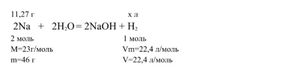
46 г Na образует 22,4 л/моль
11,27 г Na образует x л
Vтеор (H2) = х = 11,27 ∙ 22,4 / 46 = 5,488 л
4. Определим объем водорода, который был получен практически.
Vпр (H2) = Vтеор (H2) ∙ η = 5,488 ∙ 0,95 = 5,2136 л
Ответ: V(H2) = 5,2136 л.
11,27 г Na образует x л
Vтеор (H2) = х = 11,27 ∙ 22,4 / 46 = 5,488 л
4. Определим объем водорода, который был получен практически.
Vпр (H2) = Vтеор (H2) ∙ η = 5,488 ∙ 0,95 = 5,2136 л
Ответ: V(H2) = 5,2136 л.