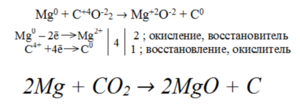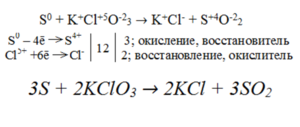Ольга «Если его умножить на 4, к произведению прибавить 8 и полученную сумму разделить
на 2, то получится 10». Обозначим за x число. Умножим на 4 ; 4x. Прибавим 8 ; 4x + 8.
Полученную сумму поделим на 2; (4x + 8)/2. И все это теперь равно 10 ; (4x + 8)/2 = 10
Развернуть задание
Используя метод электронного баланса, определите коэффициенты в схемах химических реакций.
а)Mg+ CO_2 → MgO + C
б)S + KClO_3 → KCl + SO_2
а)Mg+ CO_2 → MgO + C
б)S + KClO_3 → KCl + SO_2
Развернуть задание
Новое решение
Решение
Метод электронного баланса — один из методов уравнивания окислительно-восстановительных реакций (ОВР) заключается в том чтобы на основании степеней окисления расставить коэффициенты в ОВР. Для правильного уравнивания следует придерживаться определённой последовательности действий:
1. Найти окислитель и восстановитель – расставить степени окисления для каждого элемента, входящего в уравнение химической реакции, выделить те, которые изменяют свою степень окисления.
2. Составить для них схемы (полуреакции) переходов электронов, отвечающие данному окислительно-восстановительному процессу.
3. Уравнять число отданных и принятых электронов в полуреакциях – найти наименьшее общее кратное.
4. Расставить коэффициенты в уравнении окислительно восстановительной реакции.
а) Составим электронный баланс См. Рис.1
б) Составим электронный баланс См. Рис.2
1. Найти окислитель и восстановитель – расставить степени окисления для каждого элемента, входящего в уравнение химической реакции, выделить те, которые изменяют свою степень окисления.
2. Составить для них схемы (полуреакции) переходов электронов, отвечающие данному окислительно-восстановительному процессу.
3. Уравнять число отданных и принятых электронов в полуреакциях – найти наименьшее общее кратное.
4. Расставить коэффициенты в уравнении окислительно восстановительной реакции.
а) Составим электронный баланс См. Рис.1
б) Составим электронный баланс См. Рис.2
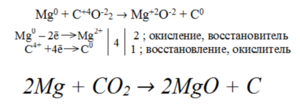
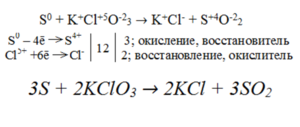
Метод электронного баланса — один из методов уравнивания окислительно-восстановительных реакций (ОВР) заключается в том чтобы на основании степеней окисления расставить коэффициенты в ОВР. Для правильного уравнивания следует придерживаться определённой последовательности действий:
1. Найти окислитель и восстановитель – расставить степени окисления для каждого элемента, входящего в уравнение химической реакции, выделить те, которые изменяют свою степень окисления.
2. Составить для них схемы (полуреакции) переходов электронов, отвечающие данному окислительно-восстановительному процессу.
3. Уравнять число отданных и принятых электронов в полуреакциях – найти наименьшее общее кратное.
4. Расставить коэффициенты в уравнении окислительно восстановительной реакции.
а) Составим электронный баланс См. Рис.1
б) Составим электронный баланс См. Рис.2
1. Найти окислитель и восстановитель – расставить степени окисления для каждого элемента, входящего в уравнение химической реакции, выделить те, которые изменяют свою степень окисления.
2. Составить для них схемы (полуреакции) переходов электронов, отвечающие данному окислительно-восстановительному процессу.
3. Уравнять число отданных и принятых электронов в полуреакциях – найти наименьшее общее кратное.
4. Расставить коэффициенты в уравнении окислительно восстановительной реакции.
а) Составим электронный баланс См. Рис.1
б) Составим электронный баланс См. Рис.2