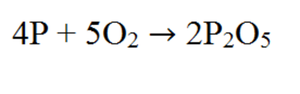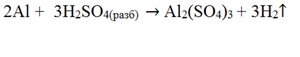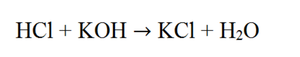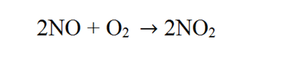Задание
Развернуть задание
Дайте полную классификационную характеристику следующих химических процессов :
а) горению фосфора;
б) взаимодействию раствора серной кислоты с алюминием;
в) реакции нейтрализации;
г) образованию оксида азота (IV) из оксида азота (II) и кислорода.
а) горению фосфора;
б) взаимодействию раствора серной кислоты с алюминием;
в) реакции нейтрализации;
г) образованию оксида азота (IV) из оксида азота (II) и кислорода.
Развернуть задание
Новое решение
Решение
Характеристика химических реакций будет происходить по такому плану :
1. Тип реакции (реакция соединения, разложения и т. д.)
2. Обратимость/необратимость.
3. Тепловой эффект (эндо-, экзотермическая).
4. Является ли ОВР (изменяются ли степени окисления).
5. Наличие или отсутствие разделов фаз (гомо-, гетерогенная).
6. Используется ли катализатор в реакции.
а) Реакция См. Рис.1
1. Реакция соединения. (из простых веществ образуется сложное)
2. Необратимая.
3. Экзотермическая (большинство реакций соединения сопровождаются выделением тепла, образуются новые связи).
4. Окислительно-восстановительная реакция, т. к. фосфор повышает степень окисления до +3, а кислород понижает до -2.
5. Реакция гетерогенная, т. к. протекает между твердым веществом и газом.
6. Некаталитическая. Реакция протекает без участия катализатора.
б) Реакция См.Рис.2
1. Реакция замещения (из исходных простого и сложного веществ получаются простое и сложное вещества нового состава).
2. Необратимая.
3. Экзотермическая реакция.
4. Окислительно-восстановительная реакция, т. к. алюминий повышает степень окисления до +3, водород понижает до 0.
5. Реакция гетерогенная, т. к. протекает между твёрдым веществом и жидкостью.
6. Некаталитическая.
в) Реакция См. Рис.3
1. Реакция обмена (из сложных веществ одного состава образуются сложные вещества другого состава).
2. Необратимая.
3. Экзотермическая (в большинстве случаев реакция нейтрализации сопровождается выделением тепла, однако бывают и эндотермические реакции. Например, реакция пищевой соды и уксусной кислоты сопровождается поглощением тепла).
4. Не является окислительно-восстановительной (степени окисления не изменяются).
5. Гомогенная, если оба реагента — растворы.
6. Некаталитическая.
г) Реакция См. Рис.4
1. Реакция соединения.
2. Необратимая.
3. Экзотермическая.
4. Окислительно-восстановительная.
5. Гомогенная, т. к. оба реагента находятся в газовом состоянии.
6. Некаталитическая (не требуется катализатор, т. к. скорость реакции довольно-таки велика при комнатной температуре).
1. Тип реакции (реакция соединения, разложения и т. д.)
2. Обратимость/необратимость.
3. Тепловой эффект (эндо-, экзотермическая).
4. Является ли ОВР (изменяются ли степени окисления).
5. Наличие или отсутствие разделов фаз (гомо-, гетерогенная).
6. Используется ли катализатор в реакции.
а) Реакция См. Рис.1
1. Реакция соединения. (из простых веществ образуется сложное)
2. Необратимая.
3. Экзотермическая (большинство реакций соединения сопровождаются выделением тепла, образуются новые связи).
4. Окислительно-восстановительная реакция, т. к. фосфор повышает степень окисления до +3, а кислород понижает до -2.
5. Реакция гетерогенная, т. к. протекает между твердым веществом и газом.
6. Некаталитическая. Реакция протекает без участия катализатора.
б) Реакция См.Рис.2
1. Реакция замещения (из исходных простого и сложного веществ получаются простое и сложное вещества нового состава).
2. Необратимая.
3. Экзотермическая реакция.
4. Окислительно-восстановительная реакция, т. к. алюминий повышает степень окисления до +3, водород понижает до 0.
5. Реакция гетерогенная, т. к. протекает между твёрдым веществом и жидкостью.
6. Некаталитическая.
в) Реакция См. Рис.3
1. Реакция обмена (из сложных веществ одного состава образуются сложные вещества другого состава).
2. Необратимая.
3. Экзотермическая (в большинстве случаев реакция нейтрализации сопровождается выделением тепла, однако бывают и эндотермические реакции. Например, реакция пищевой соды и уксусной кислоты сопровождается поглощением тепла).
4. Не является окислительно-восстановительной (степени окисления не изменяются).
5. Гомогенная, если оба реагента — растворы.
6. Некаталитическая.
г) Реакция См. Рис.4
1. Реакция соединения.
2. Необратимая.
3. Экзотермическая.
4. Окислительно-восстановительная.
5. Гомогенная, т. к. оба реагента находятся в газовом состоянии.
6. Некаталитическая (не требуется катализатор, т. к. скорость реакции довольно-таки велика при комнатной температуре).
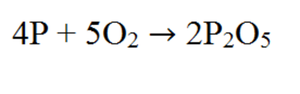
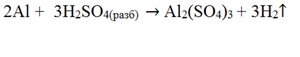
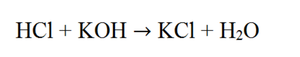
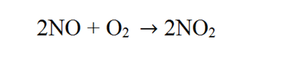
Характеристика химических реакций будет происходить по такому плану :
1. Тип реакции (реакция соединения, разложения и т. д.)
2. Обратимость/необратимость.
3. Тепловой эффект (эндо-, экзотермическая).
4. Является ли ОВР (изменяются ли степени окисления).
5. Наличие или отсутствие разделов фаз (гомо-, гетерогенная).
6. Используется ли катализатор в реакции.
а) Реакция См. Рис.1
1. Реакция соединения. (из простых веществ образуется сложное)
2. Необратимая.
3. Экзотермическая (большинство реакций соединения сопровождаются выделением тепла, образуются новые связи).
4. Окислительно-восстановительная реакция, т. к. фосфор повышает степень окисления до +3, а кислород понижает до -2.
5. Реакция гетерогенная, т. к. протекает между твердым веществом и газом.
6. Некаталитическая. Реакция протекает без участия катализатора.
б) Реакция См.Рис.2
1. Реакция замещения (из исходных простого и сложного веществ получаются простое и сложное вещества нового состава).
2. Необратимая.
3. Экзотермическая реакция.
4. Окислительно-восстановительная реакция, т. к. алюминий повышает степень окисления до +3, водород понижает до 0.
5. Реакция гетерогенная, т. к. протекает между твёрдым веществом и жидкостью.
6. Некаталитическая.
в) Реакция См. Рис.3
1. Реакция обмена (из сложных веществ одного состава образуются сложные вещества другого состава).
2. Необратимая.
3. Экзотермическая (в большинстве случаев реакция нейтрализации сопровождается выделением тепла, однако бывают и эндотермические реакции. Например, реакция пищевой соды и уксусной кислоты сопровождается поглощением тепла).
4. Не является окислительно-восстановительной (степени окисления не изменяются).
5. Гомогенная, если оба реагента — растворы.
6. Некаталитическая.
г) Реакция См. Рис.4
1. Реакция соединения.
2. Необратимая.
3. Экзотермическая.
4. Окислительно-восстановительная.
5. Гомогенная, т. к. оба реагента находятся в газовом состоянии.
6. Некаталитическая (не требуется катализатор, т. к. скорость реакции довольно-таки велика при комнатной температуре).
1. Тип реакции (реакция соединения, разложения и т. д.)
2. Обратимость/необратимость.
3. Тепловой эффект (эндо-, экзотермическая).
4. Является ли ОВР (изменяются ли степени окисления).
5. Наличие или отсутствие разделов фаз (гомо-, гетерогенная).
6. Используется ли катализатор в реакции.
а) Реакция См. Рис.1
1. Реакция соединения. (из простых веществ образуется сложное)
2. Необратимая.
3. Экзотермическая (большинство реакций соединения сопровождаются выделением тепла, образуются новые связи).
4. Окислительно-восстановительная реакция, т. к. фосфор повышает степень окисления до +3, а кислород понижает до -2.
5. Реакция гетерогенная, т. к. протекает между твердым веществом и газом.
6. Некаталитическая. Реакция протекает без участия катализатора.
б) Реакция См.Рис.2
1. Реакция замещения (из исходных простого и сложного веществ получаются простое и сложное вещества нового состава).
2. Необратимая.
3. Экзотермическая реакция.
4. Окислительно-восстановительная реакция, т. к. алюминий повышает степень окисления до +3, водород понижает до 0.
5. Реакция гетерогенная, т. к. протекает между твёрдым веществом и жидкостью.
6. Некаталитическая.
в) Реакция См. Рис.3
1. Реакция обмена (из сложных веществ одного состава образуются сложные вещества другого состава).
2. Необратимая.
3. Экзотермическая (в большинстве случаев реакция нейтрализации сопровождается выделением тепла, однако бывают и эндотермические реакции. Например, реакция пищевой соды и уксусной кислоты сопровождается поглощением тепла).
4. Не является окислительно-восстановительной (степени окисления не изменяются).
5. Гомогенная, если оба реагента — растворы.
6. Некаталитическая.
г) Реакция См. Рис.4
1. Реакция соединения.
2. Необратимая.
3. Экзотермическая.
4. Окислительно-восстановительная.
5. Гомогенная, т. к. оба реагента находятся в газовом состоянии.
6. Некаталитическая (не требуется катализатор, т. к. скорость реакции довольно-таки велика при комнатной температуре).