Развернуть задание
Вычислите объём хлора (н. у.) и массу натрия, которые можно получить при электролизе
585 г хлорида натрия, содержащего 2% примесей.
585 г хлорида натрия, содержащего 2% примесей.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
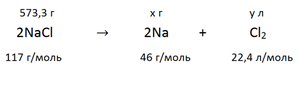
Найдем массу чистого хлорида натрия:
m (NaCl) = 585*0,98 г = 573,3 г
по пропорции
х= 573,3 г*46 г/моль/117 г/моль=225,4 г
у= 573,3 г*22,4 л/моль/117 г/моль=109,8л
Ответ: V (Cl 2 ) = 109,8 л ; m (Na) = 225,4 г
m (NaCl) = 585*0,98 г = 573,3 г
по пропорции
х= 573,3 г*46 г/моль/117 г/моль=225,4 г
у= 573,3 г*22,4 л/моль/117 г/моль=109,8л
Ответ: V (Cl 2 ) = 109,8 л ; m (Na) = 225,4 г
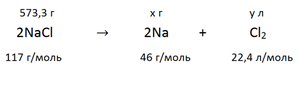
Найдем массу чистого хлорида натрия:
m (NaCl) = 585*0,98 г = 573,3 г
по пропорции
х= 573,3 г*46 г/моль/117 г/моль=225,4 г
у= 573,3 г*22,4 л/моль/117 г/моль=109,8л
Ответ: V (Cl 2 ) = 109,8 л ; m (Na) = 225,4 г
m (NaCl) = 585*0,98 г = 573,3 г
по пропорции
х= 573,3 г*46 г/моль/117 г/моль=225,4 г
у= 573,3 г*22,4 л/моль/117 г/моль=109,8л
Ответ: V (Cl 2 ) = 109,8 л ; m (Na) = 225,4 г