Ира М(С4Н10) = 4*12 + 10*1 = 58 г/моль
ω(C) = 4*12 / 58*100% = 82,8%
М(С5Н12) = 5*12 + 12*1 = 72 г/моль
ω (C) = 5*12 / 72*100% = 83,3%
Задание
Развернуть задание
Написать уравнения реакций, с помощью которых можно осуществить следующие превращения:
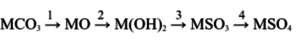
Какие металлы главной подгруппы II группы Периодической системы Д.И.Менделеева могут быть использованы для этих превращений, а какие – нет? Почему?
Развернуть задание
Новое решение
Решение
1) MCO3 = MO + CO2 ↑
2) MO + H2O = M(OH)2
3) M(OH)2 + Na2SO3 = MSO3 + 2NaOH
4) MSO3 + H2SO4 = MSO4 + H2O + SO2 ↑
В качестве металлов можно использовать Ba и Ca. Это щелочноземельные металлы и они образуют растворимые основания, которые могут быть получены взаимодействием оксидов этих металлов с водой. Mg и Be образуют нерастворимые основания, которые нельзя получить взаимодействием их оксидов с водой.
2) MO + H2O = M(OH)2
3) M(OH)2 + Na2SO3 = MSO3 + 2NaOH
4) MSO3 + H2SO4 = MSO4 + H2O + SO2 ↑
В качестве металлов можно использовать Ba и Ca. Это щелочноземельные металлы и они образуют растворимые основания, которые могут быть получены взаимодействием оксидов этих металлов с водой. Mg и Be образуют нерастворимые основания, которые нельзя получить взаимодействием их оксидов с водой.
1) MCO3 = MO + CO2 ↑
2) MO + H2O = M(OH)2
3) M(OH)2 + Na2SO3 = MSO3 + 2NaOH
4) MSO3 + H2SO4 = MSO4 + H2O + SO2 ↑
В качестве металлов можно использовать Ba и Ca. Это щелочноземельные металлы и они образуют растворимые основания, которые могут быть получены взаимодействием оксидов этих металлов с водой. Mg и Be образуют нерастворимые основания, которые нельзя получить взаимодействием их оксидов с водой.
2) MO + H2O = M(OH)2
3) M(OH)2 + Na2SO3 = MSO3 + 2NaOH
4) MSO3 + H2SO4 = MSO4 + H2O + SO2 ↑
В качестве металлов можно использовать Ba и Ca. Это щелочноземельные металлы и они образуют растворимые основания, которые могут быть получены взаимодействием оксидов этих металлов с водой. Mg и Be образуют нерастворимые основания, которые нельзя получить взаимодействием их оксидов с водой.