Задание
Развернуть задание
Вычислить объем водорода (н.у.), который может быть получен при растворении в едком натре 270 мг сплава, содержащего 5% меди. Выход водорода принять равным 85% от теоретически возможного.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
Дано:
m (сплава Al+Cu) = 270 мг = 0,27 г
ω(Сu) = 5%
η = 85 % или 0,85
V пр (H2) - ?
Решение:
1. Составим уравнение реакции. Из двух компонентов, входящих в состав сплава, в едком натре будет растворяться только алюминий:
m (сплава Al+Cu) = 270 мг = 0,27 г
ω(Сu) = 5%
η = 85 % или 0,85
V пр (H2) - ?
Решение:
1. Составим уравнение реакции. Из двух компонентов, входящих в состав сплава, в едком натре будет растворяться только алюминий:
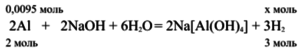
2. Рассчитаем массовую долю алюминия в сплаве:
ω(Al) = 100% - ω(Cu) = 100% - 5% = 95% или 0,95
3. Для нахождения массы алюминия в сплаве можно использовать
следующую формулу:
ω(Al) = 100% - ω(Cu) = 100% - 5% = 95% или 0,95
3. Для нахождения массы алюминия в сплаве можно использовать
следующую формулу:
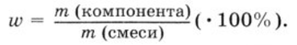
m(Al) = m(сплава) ∙ ω(Al) = 0,27 ∙ 0,95 = 0,257 г
4. Вычислим количество вещества алюминия по формуле:
4. Вычислим количество вещества алюминия по формуле:
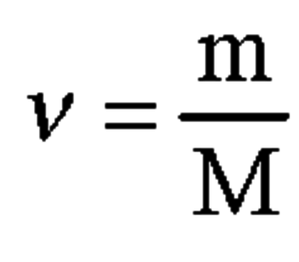
M(Al) = 27 г/моль
n(Al) = 0,257 / 27 = 0,0095 моль
5. По уравнению реакции из 2 моль алюминия образуется 3 моль водорода. Тогда, из 0,0095 моль алюминия образуется в 1,5 раза большее количество водорода:
n(H2) = 0,0095 ∙3 / 2 = 0,01425 моль
6. Найдем объема водорода, который теоретически должен был получиться в ходе реакции:
V теор (H2) = (Vm) ∙ n = 0,01425 ∙ 22,4 = 0,3192 л
7. Определим объем водорода, который был получен практически. Так как выход газа составляет 85% от теоретически возможного, то можно воспользоваться формулой:
n(Al) = 0,257 / 27 = 0,0095 моль
5. По уравнению реакции из 2 моль алюминия образуется 3 моль водорода. Тогда, из 0,0095 моль алюминия образуется в 1,5 раза большее количество водорода:
n(H2) = 0,0095 ∙3 / 2 = 0,01425 моль
6. Найдем объема водорода, который теоретически должен был получиться в ходе реакции:
V теор (H2) = (Vm) ∙ n = 0,01425 ∙ 22,4 = 0,3192 л
7. Определим объем водорода, который был получен практически. Так как выход газа составляет 85% от теоретически возможного, то можно воспользоваться формулой:

Vпр (H2) = Vтеор (H2) ∙ η = 0,3192 ∙ 0,85 = 0,271 л = 271 мл
Ответ: Vпр (H2) = 271 мл.
Ответ: Vпр (H2) = 271 мл.
Дано:
m (сплава Al+Cu) = 270 мг = 0,27 г
ω(Сu) = 5%
η = 85 % или 0,85
V пр (H2) - ?
Решение:
1. Составим уравнение реакции. Из двух компонентов, входящих в состав сплава, в едком натре будет растворяться только алюминий:
m (сплава Al+Cu) = 270 мг = 0,27 г
ω(Сu) = 5%
η = 85 % или 0,85
V пр (H2) - ?
Решение:
1. Составим уравнение реакции. Из двух компонентов, входящих в состав сплава, в едком натре будет растворяться только алюминий:
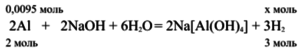
2. Рассчитаем массовую долю алюминия в сплаве:
ω(Al) = 100% - ω(Cu) = 100% - 5% = 95% или 0,95
3. Для нахождения массы алюминия в сплаве можно использовать
следующую формулу:
ω(Al) = 100% - ω(Cu) = 100% - 5% = 95% или 0,95
3. Для нахождения массы алюминия в сплаве можно использовать
следующую формулу:
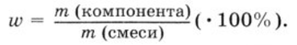
m(Al) = m(сплава) ∙ ω(Al) = 0,27 ∙ 0,95 = 0,257 г
4. Вычислим количество вещества алюминия по формуле:
4. Вычислим количество вещества алюминия по формуле:
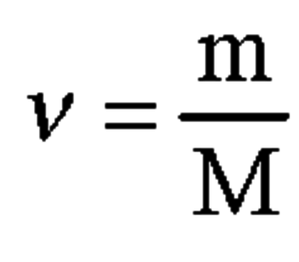
M(Al) = 27 г/моль
n(Al) = 0,257 / 27 = 0,0095 моль
5. По уравнению реакции из 2 моль алюминия образуется 3 моль водорода. Тогда, из 0,0095 моль алюминия образуется в 1,5 раза большее количество водорода:
n(H2) = 0,0095 ∙3 / 2 = 0,01425 моль
6. Найдем объема водорода, который теоретически должен был получиться в ходе реакции:
V теор (H2) = (Vm) ∙ n = 0,01425 ∙ 22,4 = 0,3192 л
7. Определим объем водорода, который был получен практически. Так как выход газа составляет 85% от теоретически возможного, то можно воспользоваться формулой:
n(Al) = 0,257 / 27 = 0,0095 моль
5. По уравнению реакции из 2 моль алюминия образуется 3 моль водорода. Тогда, из 0,0095 моль алюминия образуется в 1,5 раза большее количество водорода:
n(H2) = 0,0095 ∙3 / 2 = 0,01425 моль
6. Найдем объема водорода, который теоретически должен был получиться в ходе реакции:
V теор (H2) = (Vm) ∙ n = 0,01425 ∙ 22,4 = 0,3192 л
7. Определим объем водорода, который был получен практически. Так как выход газа составляет 85% от теоретически возможного, то можно воспользоваться формулой:

Vпр (H2) = Vтеор (H2) ∙ η = 0,3192 ∙ 0,85 = 0,271 л = 271 мл
Ответ: Vпр (H2) = 271 мл.
Ответ: Vпр (H2) = 271 мл.