Развернуть задание
Вычислите объём сернистого газа (н. у.), который образуется при обжиге 485 кг цинковой
обманки, содержащей в качестве примеси 20% оксида кремния (IV).
обманки, содержащей в качестве примеси 20% оксида кремния (IV).
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
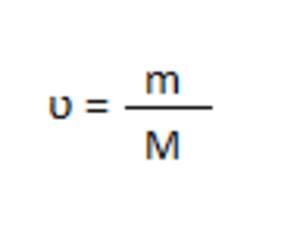
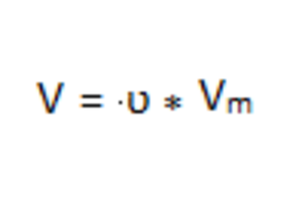
Дано:
m (ZnS) = 485 кг
ω (SiO 2 ) =20%
Найти:
V (SO 2 ) - ?
Решение:
2ZnS + 3О 2 = 2SO 2 + 2ZnО
Переведем массу цинковой обманки из кг в г:
m (ZnS) = 485 кг * 1000 = 485 * 10 3 г
Найдем массу примеси:
m пр. = 485 * 10 3 г * 0,2 = 97 * 10 3 г
Найдем массу чистого сульфида цинка:
m (ZnS) = 485 * 10 3 г - 97 * 10 3 г = 388 * 10 3 г
Рассчитаем молярную массу и количество вещества (по формуле: 1)
цинковой обманки:
М (ZnS) = 65 +32 = 97 г/моль
ʋ (ZnS) = 388 * 10 3 г / 97 г/моль = 4 * 10 3 моль
Найдем количество вещества сернистого газа:
ʋ (SO 2 ) : ʋ (ZnS) = 2:2 = 1:1 из этого следует, что ʋ (SO 2 ) = ʋ (ZnS) = 4 * 10 3 моль
Рассчитаем объем сернистого газа по формуле: 2
V (SO 2 ) = 4 * 10 3 моль * 22,4 л/моль = 89,6 * 10 3 л
Ответ: V (SO 2 ) = 89,6 * 10 3 л
m (ZnS) = 485 кг
ω (SiO 2 ) =20%
Найти:
V (SO 2 ) - ?
Решение:
2ZnS + 3О 2 = 2SO 2 + 2ZnО
Переведем массу цинковой обманки из кг в г:
m (ZnS) = 485 кг * 1000 = 485 * 10 3 г
Найдем массу примеси:
m пр. = 485 * 10 3 г * 0,2 = 97 * 10 3 г
Найдем массу чистого сульфида цинка:
m (ZnS) = 485 * 10 3 г - 97 * 10 3 г = 388 * 10 3 г
Рассчитаем молярную массу и количество вещества (по формуле: 1)
цинковой обманки:
М (ZnS) = 65 +32 = 97 г/моль
ʋ (ZnS) = 388 * 10 3 г / 97 г/моль = 4 * 10 3 моль
Найдем количество вещества сернистого газа:
ʋ (SO 2 ) : ʋ (ZnS) = 2:2 = 1:1 из этого следует, что ʋ (SO 2 ) = ʋ (ZnS) = 4 * 10 3 моль
Рассчитаем объем сернистого газа по формуле: 2
V (SO 2 ) = 4 * 10 3 моль * 22,4 л/моль = 89,6 * 10 3 л
Ответ: V (SO 2 ) = 89,6 * 10 3 л
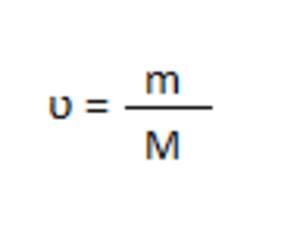
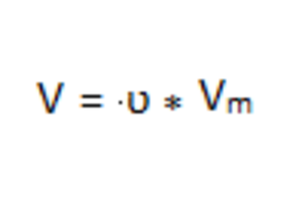
Дано:
m (ZnS) = 485 кг
ω (SiO 2 ) =20%
Найти:
V (SO 2 ) - ?
Решение:
2ZnS + 3О 2 = 2SO 2 + 2ZnО
Переведем массу цинковой обманки из кг в г:
m (ZnS) = 485 кг * 1000 = 485 * 10 3 г
Найдем массу примеси:
m пр. = 485 * 10 3 г * 0,2 = 97 * 10 3 г
Найдем массу чистого сульфида цинка:
m (ZnS) = 485 * 10 3 г - 97 * 10 3 г = 388 * 10 3 г
Рассчитаем молярную массу и количество вещества (по формуле: 1)
цинковой обманки:
М (ZnS) = 65 +32 = 97 г/моль
ʋ (ZnS) = 388 * 10 3 г / 97 г/моль = 4 * 10 3 моль
Найдем количество вещества сернистого газа:
ʋ (SO 2 ) : ʋ (ZnS) = 2:2 = 1:1 из этого следует, что ʋ (SO 2 ) = ʋ (ZnS) = 4 * 10 3 моль
Рассчитаем объем сернистого газа по формуле: 2
V (SO 2 ) = 4 * 10 3 моль * 22,4 л/моль = 89,6 * 10 3 л
Ответ: V (SO 2 ) = 89,6 * 10 3 л
m (ZnS) = 485 кг
ω (SiO 2 ) =20%
Найти:
V (SO 2 ) - ?
Решение:
2ZnS + 3О 2 = 2SO 2 + 2ZnО
Переведем массу цинковой обманки из кг в г:
m (ZnS) = 485 кг * 1000 = 485 * 10 3 г
Найдем массу примеси:
m пр. = 485 * 10 3 г * 0,2 = 97 * 10 3 г
Найдем массу чистого сульфида цинка:
m (ZnS) = 485 * 10 3 г - 97 * 10 3 г = 388 * 10 3 г
Рассчитаем молярную массу и количество вещества (по формуле: 1)
цинковой обманки:
М (ZnS) = 65 +32 = 97 г/моль
ʋ (ZnS) = 388 * 10 3 г / 97 г/моль = 4 * 10 3 моль
Найдем количество вещества сернистого газа:
ʋ (SO 2 ) : ʋ (ZnS) = 2:2 = 1:1 из этого следует, что ʋ (SO 2 ) = ʋ (ZnS) = 4 * 10 3 моль
Рассчитаем объем сернистого газа по формуле: 2
V (SO 2 ) = 4 * 10 3 моль * 22,4 л/моль = 89,6 * 10 3 л
Ответ: V (SO 2 ) = 89,6 * 10 3 л