Задание
Развернуть задание
Вычислить объем оксида углерода (II) (н.у.), который потребуется для восстановления железа из 2,32 т магнитного железняка, содержащего 5% пустой породы. Вычислить количество вещества железа, которое при этом получится, если выход его составляет 80% от теоретически возможного.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
Дано:
m(т.Fe3O4) = 2,32 т
ω(прим.) = 5%
η = 80 % или 0,8
V(CO) - ?
n_пр (Fe)-?
Решение:
1. Составим уравнение реакции восстановления железа из магнитного железняка Fe3O4:
m(т.Fe3O4) = 2,32 т
ω(прим.) = 5%
η = 80 % или 0,8
V(CO) - ?
n_пр (Fe)-?
Решение:
1. Составим уравнение реакции восстановления железа из магнитного железняка Fe3O4:
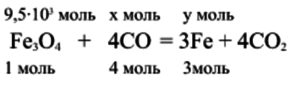
2. Рассчитаем массовую долю Fe3O4 в горной породе:
ω(Fe3O4) = 100% - ω(Fe3O4) = 100% - 5% = 95% или 0,95
3. Для нахождения массы Fe3O4 в горной породе можно использовать следующую формулу:
ω(Fe3O4) = 100% - ω(Fe3O4) = 100% - 5% = 95% или 0,95
3. Для нахождения массы Fe3O4 в горной породе можно использовать следующую формулу:
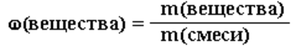
m(Fe3O4) = m(т. Fe3O4) ∙ ω(Fe3O4) = 2,32 ∙ 0,95 = 2,204 т =
2,204∙10^6 г
4. Вычислим количество вещества Fe3O4 по формуле:
2,204∙10^6 г
4. Вычислим количество вещества Fe3O4 по формуле:
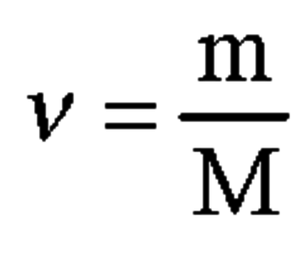
M(Fe3O4) = 232 г/моль
n(Fe3O4) = 2,204∙10^6 / 232 = 9500 моль = 9,5∙10^3 моль
5. По уравнению реакции для восстановления 1 моль Fe3O4 необходимо 4 моль СО. Тогда, для восстановления 9,5∙10^3 моль Fe3O4 необходимо в 4 раза большее количество СО:
n(СО) = 9,5∙10^3 ∙ 4 = 3,8∙10^4 моль
6. Так как условия нормальные, можно вычислить объем СО, используя мольный объем:
V(CO)= n(CO) ∙ Vm = 3,8∙10^4 ∙ 22,4 = 8,512 ∙ 10^5 л
7. Найдем количество вещества железа, которое теоретически должно было получиться в ходе реакции. По уравнению реакции из 1 моль Fe3O4 образуется 3 моль Fe, тогда из 9,5∙10^3 моль
Fe3O4 образуется в 3 раза большее количество Fe:
n_теор (Fe) = 9,5∙10^3 ∙ 3 = 2,85∙10^4 моль
8. Определим количество вещества железа, которое было получено практически.
n_пр (Fe) = n_теор (Fe) ∙ η = 2,85∙10^4 ∙ 0,8 = 2,28∙10^4 моль
Ответ: V(СО) = 8,512 ∙ 10^5 л, n_пр (Fe) = 2,28∙10^4 моль
n(Fe3O4) = 2,204∙10^6 / 232 = 9500 моль = 9,5∙10^3 моль
5. По уравнению реакции для восстановления 1 моль Fe3O4 необходимо 4 моль СО. Тогда, для восстановления 9,5∙10^3 моль Fe3O4 необходимо в 4 раза большее количество СО:
n(СО) = 9,5∙10^3 ∙ 4 = 3,8∙10^4 моль
6. Так как условия нормальные, можно вычислить объем СО, используя мольный объем:
V(CO)= n(CO) ∙ Vm = 3,8∙10^4 ∙ 22,4 = 8,512 ∙ 10^5 л
7. Найдем количество вещества железа, которое теоретически должно было получиться в ходе реакции. По уравнению реакции из 1 моль Fe3O4 образуется 3 моль Fe, тогда из 9,5∙10^3 моль
Fe3O4 образуется в 3 раза большее количество Fe:
n_теор (Fe) = 9,5∙10^3 ∙ 3 = 2,85∙10^4 моль
8. Определим количество вещества железа, которое было получено практически.
n_пр (Fe) = n_теор (Fe) ∙ η = 2,85∙10^4 ∙ 0,8 = 2,28∙10^4 моль
Ответ: V(СО) = 8,512 ∙ 10^5 л, n_пр (Fe) = 2,28∙10^4 моль
Дано:
m(т.Fe3O4) = 2,32 т
ω(прим.) = 5%
η = 80 % или 0,8
V(CO) - ?
n_пр (Fe)-?
Решение:
1. Составим уравнение реакции восстановления железа из магнитного железняка Fe3O4:
m(т.Fe3O4) = 2,32 т
ω(прим.) = 5%
η = 80 % или 0,8
V(CO) - ?
n_пр (Fe)-?
Решение:
1. Составим уравнение реакции восстановления железа из магнитного железняка Fe3O4:
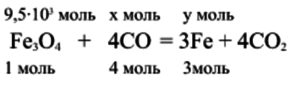
2. Рассчитаем массовую долю Fe3O4 в горной породе:
ω(Fe3O4) = 100% - ω(Fe3O4) = 100% - 5% = 95% или 0,95
3. Для нахождения массы Fe3O4 в горной породе можно использовать следующую формулу:
ω(Fe3O4) = 100% - ω(Fe3O4) = 100% - 5% = 95% или 0,95
3. Для нахождения массы Fe3O4 в горной породе можно использовать следующую формулу:
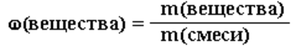
m(Fe3O4) = m(т. Fe3O4) ∙ ω(Fe3O4) = 2,32 ∙ 0,95 = 2,204 т =
2,204∙10^6 г
4. Вычислим количество вещества Fe3O4 по формуле:
2,204∙10^6 г
4. Вычислим количество вещества Fe3O4 по формуле:
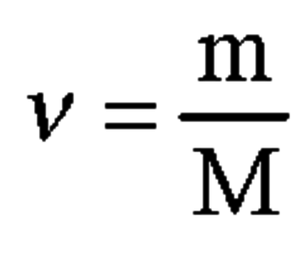
M(Fe3O4) = 232 г/моль
n(Fe3O4) = 2,204∙10^6 / 232 = 9500 моль = 9,5∙10^3 моль
5. По уравнению реакции для восстановления 1 моль Fe3O4 необходимо 4 моль СО. Тогда, для восстановления 9,5∙10^3 моль Fe3O4 необходимо в 4 раза большее количество СО:
n(СО) = 9,5∙10^3 ∙ 4 = 3,8∙10^4 моль
6. Так как условия нормальные, можно вычислить объем СО, используя мольный объем:
V(CO)= n(CO) ∙ Vm = 3,8∙10^4 ∙ 22,4 = 8,512 ∙ 10^5 л
7. Найдем количество вещества железа, которое теоретически должно было получиться в ходе реакции. По уравнению реакции из 1 моль Fe3O4 образуется 3 моль Fe, тогда из 9,5∙10^3 моль
Fe3O4 образуется в 3 раза большее количество Fe:
n_теор (Fe) = 9,5∙10^3 ∙ 3 = 2,85∙10^4 моль
8. Определим количество вещества железа, которое было получено практически.
n_пр (Fe) = n_теор (Fe) ∙ η = 2,85∙10^4 ∙ 0,8 = 2,28∙10^4 моль
Ответ: V(СО) = 8,512 ∙ 10^5 л, n_пр (Fe) = 2,28∙10^4 моль
n(Fe3O4) = 2,204∙10^6 / 232 = 9500 моль = 9,5∙10^3 моль
5. По уравнению реакции для восстановления 1 моль Fe3O4 необходимо 4 моль СО. Тогда, для восстановления 9,5∙10^3 моль Fe3O4 необходимо в 4 раза большее количество СО:
n(СО) = 9,5∙10^3 ∙ 4 = 3,8∙10^4 моль
6. Так как условия нормальные, можно вычислить объем СО, используя мольный объем:
V(CO)= n(CO) ∙ Vm = 3,8∙10^4 ∙ 22,4 = 8,512 ∙ 10^5 л
7. Найдем количество вещества железа, которое теоретически должно было получиться в ходе реакции. По уравнению реакции из 1 моль Fe3O4 образуется 3 моль Fe, тогда из 9,5∙10^3 моль
Fe3O4 образуется в 3 раза большее количество Fe:
n_теор (Fe) = 9,5∙10^3 ∙ 3 = 2,85∙10^4 моль
8. Определим количество вещества железа, которое было получено практически.
n_пр (Fe) = n_теор (Fe) ∙ η = 2,85∙10^4 ∙ 0,8 = 2,28∙10^4 моль
Ответ: V(СО) = 8,512 ∙ 10^5 л, n_пр (Fe) = 2,28∙10^4 моль