Задание
Развернуть задание
Сколько килограммов 68%-й азотной кислоты можно получить из 276 кг(н. у.) оксида азота (IV)?
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
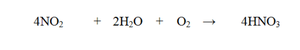
По уравнению n(NO 2 )=n(HNO 3 )= 276 кг/46(кг/кмоль)=6кмоль
m(HNO 3 )=6 кмоль*63 кг/кмоль=378 кг
Вычислим массу раствора азотной кислоты :
Воспользуемся формулой :
m(HNO 3 )=6 кмоль*63 кг/кмоль=378 кг
Вычислим массу раствора азотной кислоты :
Воспользуемся формулой :
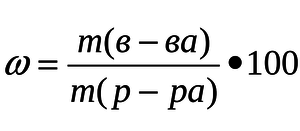
m(HNO 3 )= 378 кг/0,68 = 556 кг
Ответ : 556 кг
Ответ : 556 кг
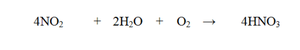
По уравнению n(NO 2 )=n(HNO 3 )= 276 кг/46(кг/кмоль)=6кмоль
m(HNO 3 )=6 кмоль*63 кг/кмоль=378 кг
Вычислим массу раствора азотной кислоты :
Воспользуемся формулой :
m(HNO 3 )=6 кмоль*63 кг/кмоль=378 кг
Вычислим массу раствора азотной кислоты :
Воспользуемся формулой :
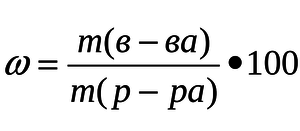
m(HNO 3 )= 378 кг/0,68 = 556 кг
Ответ : 556 кг
Ответ : 556 кг