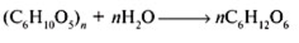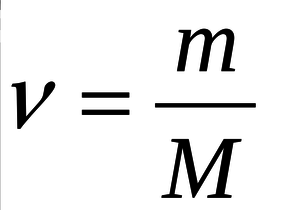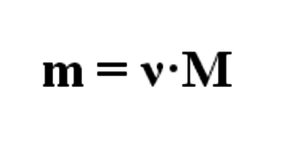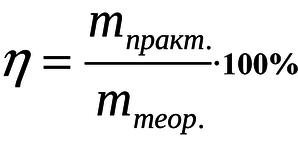Задание
Развернуть задание
Гидролизом 250 кг древесных опилок, содержание целлюлозы в которых составляет 45%, было получено 62 кг глюкозы. Определите массовую долю выхода глюкозы от теоретически возможного.
Развернуть задание
Новое решение
Решение
Дано:
m(опилок) = 250 кг
ω((C(6)H(10)O(5))(n)) = 45%
m(С(6)H(12)O(6)) = 62 кг
ηвых(C(6)H(12)O(6)) - ?
Решение:
Из формулы на 2 картинке следует, что масса вычисляется по формуле, представленной на 3 картинке, где ω – массовая доля
вещества)
m((C(6)H(10)O(5))(n)) = (250 кг/ 100%) * 45% = 112,5 кг
По формуле на 4 картинке, где ν – количество вещества, m- масса вещества, M- молярная масса вещества) найдем количество вещества целлюлозы
ν((C(6)H(10)O(5))(n)) = 112,5 кг/(162 кг/кмоль * n) = 0,69/n кмоль
Из реакции видно, что количество глюкозы в n раз больше количества целлюлозы
ν(C(6)H(12)O(6)) = n * ν((C(6)H(10)O(5))(n)) = 0,69 кмоль
Найдем теоретическую массу глюкозы по формуле на 5 картинке
mтеор(C(6)H(12)O(6)) = 0,69 кмоль * 180 кг/кмоль = 124,2 кг
Найдем массовую долю выхода η глюкозы по формуле, представленной на 6 картинке
ηвых(C(6)H(12)O(6)) = (62 кг/124,2 кг) * 100% = 49,9%
Ответ: 49,9%
m(опилок) = 250 кг
ω((C(6)H(10)O(5))(n)) = 45%
m(С(6)H(12)O(6)) = 62 кг
ηвых(C(6)H(12)O(6)) - ?
Решение:
Из формулы на 2 картинке следует, что масса вычисляется по формуле, представленной на 3 картинке, где ω – массовая доля
вещества)
m((C(6)H(10)O(5))(n)) = (250 кг/ 100%) * 45% = 112,5 кг
По формуле на 4 картинке, где ν – количество вещества, m- масса вещества, M- молярная масса вещества) найдем количество вещества целлюлозы
ν((C(6)H(10)O(5))(n)) = 112,5 кг/(162 кг/кмоль * n) = 0,69/n кмоль
Из реакции видно, что количество глюкозы в n раз больше количества целлюлозы
ν(C(6)H(12)O(6)) = n * ν((C(6)H(10)O(5))(n)) = 0,69 кмоль
Найдем теоретическую массу глюкозы по формуле на 5 картинке
mтеор(C(6)H(12)O(6)) = 0,69 кмоль * 180 кг/кмоль = 124,2 кг
Найдем массовую долю выхода η глюкозы по формуле, представленной на 6 картинке
ηвых(C(6)H(12)O(6)) = (62 кг/124,2 кг) * 100% = 49,9%
Ответ: 49,9%
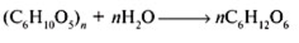


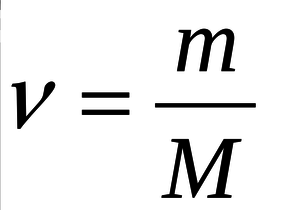
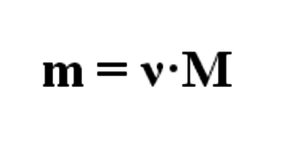
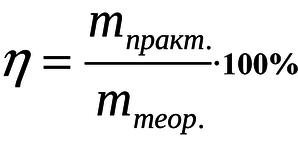
Дано:
m(опилок) = 250 кг
ω((C(6)H(10)O(5))(n)) = 45%
m(С(6)H(12)O(6)) = 62 кг
ηвых(C(6)H(12)O(6)) - ?
Решение:
Из формулы на 2 картинке следует, что масса вычисляется по формуле, представленной на 3 картинке, где ω – массовая доля
вещества)
m((C(6)H(10)O(5))(n)) = (250 кг/ 100%) * 45% = 112,5 кг
По формуле на 4 картинке, где ν – количество вещества, m- масса вещества, M- молярная масса вещества) найдем количество вещества целлюлозы
ν((C(6)H(10)O(5))(n)) = 112,5 кг/(162 кг/кмоль * n) = 0,69/n кмоль
Из реакции видно, что количество глюкозы в n раз больше количества целлюлозы
ν(C(6)H(12)O(6)) = n * ν((C(6)H(10)O(5))(n)) = 0,69 кмоль
Найдем теоретическую массу глюкозы по формуле на 5 картинке
mтеор(C(6)H(12)O(6)) = 0,69 кмоль * 180 кг/кмоль = 124,2 кг
Найдем массовую долю выхода η глюкозы по формуле, представленной на 6 картинке
ηвых(C(6)H(12)O(6)) = (62 кг/124,2 кг) * 100% = 49,9%
Ответ: 49,9%
m(опилок) = 250 кг
ω((C(6)H(10)O(5))(n)) = 45%
m(С(6)H(12)O(6)) = 62 кг
ηвых(C(6)H(12)O(6)) - ?
Решение:
Из формулы на 2 картинке следует, что масса вычисляется по формуле, представленной на 3 картинке, где ω – массовая доля
вещества)
m((C(6)H(10)O(5))(n)) = (250 кг/ 100%) * 45% = 112,5 кг
По формуле на 4 картинке, где ν – количество вещества, m- масса вещества, M- молярная масса вещества) найдем количество вещества целлюлозы
ν((C(6)H(10)O(5))(n)) = 112,5 кг/(162 кг/кмоль * n) = 0,69/n кмоль
Из реакции видно, что количество глюкозы в n раз больше количества целлюлозы
ν(C(6)H(12)O(6)) = n * ν((C(6)H(10)O(5))(n)) = 0,69 кмоль
Найдем теоретическую массу глюкозы по формуле на 5 картинке
mтеор(C(6)H(12)O(6)) = 0,69 кмоль * 180 кг/кмоль = 124,2 кг
Найдем массовую долю выхода η глюкозы по формуле, представленной на 6 картинке
ηвых(C(6)H(12)O(6)) = (62 кг/124,2 кг) * 100% = 49,9%
Ответ: 49,9%