Развернуть задание
Вычислите массу соли, которую можно получить при взаимодействии 150 г 5%-го раствора аминоуксусной кислоты с необходимым количеством гидроксида натрия. Сколько граммов 12%-го раствора щелочи потребуется для реакции?
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
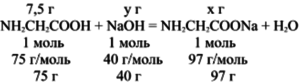
m(NH2 CH2 COOH) = (150 г/ 100%) ∙ 5% = 7,5 г
По уравнению реакции из 75 г аминоуксусной кислоты образуется 97 г соли, тогда из 7,5 г образуется х г соли.
х = m(NH2 CH2 COONa) = 7,5 ∙ 97 / 75 = 9,7 г
По уравнению реакции 75 г аминоуксусной кислоты вступает в реакцию с 40 г NaOH, тогда 7,5 г кислоты вступит в реакцию c y г NaOH.
y = m(NaOH) = 7,5 ∙ 40 / 75 = 4 г
m р (NaOH) = (4 г/ 12%) ∙ 100% = 33,3 г
Ответ: m(NH2 CH2 COONa) = 9,7 г; m р (NaOH) = 33,3 г
По уравнению реакции из 75 г аминоуксусной кислоты образуется 97 г соли, тогда из 7,5 г образуется х г соли.
х = m(NH2 CH2 COONa) = 7,5 ∙ 97 / 75 = 9,7 г
По уравнению реакции 75 г аминоуксусной кислоты вступает в реакцию с 40 г NaOH, тогда 7,5 г кислоты вступит в реакцию c y г NaOH.
y = m(NaOH) = 7,5 ∙ 40 / 75 = 4 г
m р (NaOH) = (4 г/ 12%) ∙ 100% = 33,3 г
Ответ: m(NH2 CH2 COONa) = 9,7 г; m р (NaOH) = 33,3 г
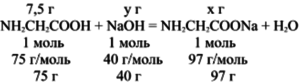
m(NH2 CH2 COOH) = (150 г/ 100%) ∙ 5% = 7,5 г
По уравнению реакции из 75 г аминоуксусной кислоты образуется 97 г соли, тогда из 7,5 г образуется х г соли.
х = m(NH2 CH2 COONa) = 7,5 ∙ 97 / 75 = 9,7 г
По уравнению реакции 75 г аминоуксусной кислоты вступает в реакцию с 40 г NaOH, тогда 7,5 г кислоты вступит в реакцию c y г NaOH.
y = m(NaOH) = 7,5 ∙ 40 / 75 = 4 г
m р (NaOH) = (4 г/ 12%) ∙ 100% = 33,3 г
Ответ: m(NH2 CH2 COONa) = 9,7 г; m р (NaOH) = 33,3 г
По уравнению реакции из 75 г аминоуксусной кислоты образуется 97 г соли, тогда из 7,5 г образуется х г соли.
х = m(NH2 CH2 COONa) = 7,5 ∙ 97 / 75 = 9,7 г
По уравнению реакции 75 г аминоуксусной кислоты вступает в реакцию с 40 г NaOH, тогда 7,5 г кислоты вступит в реакцию c y г NaOH.
y = m(NaOH) = 7,5 ∙ 40 / 75 = 4 г
m р (NaOH) = (4 г/ 12%) ∙ 100% = 33,3 г
Ответ: m(NH2 CH2 COONa) = 9,7 г; m р (NaOH) = 33,3 г