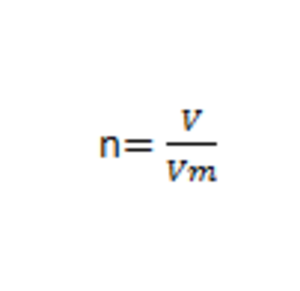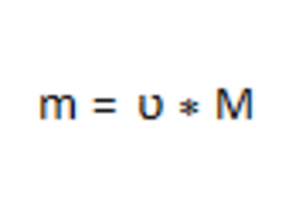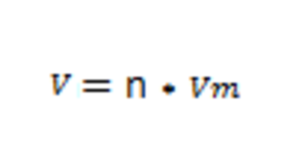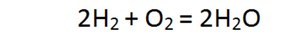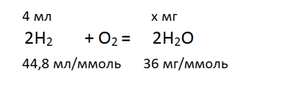Развернуть задание
В стеклянном толстостенном сосуде (эвдиометре) взорвали смесь 4 мл водорода и 3 мл
кислорода. Найдите массу продукта реакции и объём непрореагировавшего газа.
кислорода. Найдите массу продукта реакции и объём непрореагировавшего газа.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
Дано:
V(O 2 ) = 3 мл
V(H 2 ) = 4 мл
Найти:
m (H 2 O) - ?
V непр.г - ?
Решение:
Уравнение реакции 4
Вычислим количество вещества кислорода и водорода по формуле: 1
n (O 2 ) = 3 мл / 22,4 мл/ммоль = 0, 13 ммоль
n (H 2 ) = 4 мл / 22,4 мл/ммоль = 0, 18 ммоль
Найдем какое вещество находится в избытке, а какое в недостатке. Определяем сколько
для реакции необходимо водорода. Слева пишем теоретические количества вещества, а
справа практические количества вещества:
2 моль (H 2 ) – х (H 2 )
1 моль (O 2 ) – 0, 13 ммоль
Находим х:
х = (2 моль * 0,13 ммоль) / 1 моль = 0,26 ммоль
Видно, что водород находится в недостатке, следовательно, считаем по водороду
количество вещества воды:
n (H 2 O) : n (H 2 ) = 1:1 из этого следует, что n (H 2 O) = n (H 2 ) = 0,18 ммоль
Вычислим массу воды по формуле: 2
М (H 2 O) = 2 * 1 + 16 = 18 мг/ммоль
m (H 2 O) = 18 мг/ммоль * 0,18 ммоль = 3,2 мг
Найдем количество вещества непрореагировавшего газа:
n неп = 0,13 ммоль – 0,09 ммоль = 0,04 ммоль
Рассчитаем объем непрореагировавшего газа по формуле: 3
V нер.г = 0,04 моль * 22,4 мл/ммоль = 0,9 мл
Ответ: V нер.г = 0,9 мл; m (H 2 O) = 3,2 мг
V(O 2 ) = 3 мл
V(H 2 ) = 4 мл
Найти:
m (H 2 O) - ?
V непр.г - ?
Решение:
Уравнение реакции 4
Вычислим количество вещества кислорода и водорода по формуле: 1
n (O 2 ) = 3 мл / 22,4 мл/ммоль = 0, 13 ммоль
n (H 2 ) = 4 мл / 22,4 мл/ммоль = 0, 18 ммоль
Найдем какое вещество находится в избытке, а какое в недостатке. Определяем сколько
для реакции необходимо водорода. Слева пишем теоретические количества вещества, а
справа практические количества вещества:
2 моль (H 2 ) – х (H 2 )
1 моль (O 2 ) – 0, 13 ммоль
Находим х:
х = (2 моль * 0,13 ммоль) / 1 моль = 0,26 ммоль
Видно, что водород находится в недостатке, следовательно, считаем по водороду
количество вещества воды:
n (H 2 O) : n (H 2 ) = 1:1 из этого следует, что n (H 2 O) = n (H 2 ) = 0,18 ммоль
Вычислим массу воды по формуле: 2
М (H 2 O) = 2 * 1 + 16 = 18 мг/ммоль
m (H 2 O) = 18 мг/ммоль * 0,18 ммоль = 3,2 мг
Найдем количество вещества непрореагировавшего газа:
n неп = 0,13 ммоль – 0,09 ммоль = 0,04 ммоль
Рассчитаем объем непрореагировавшего газа по формуле: 3
V нер.г = 0,04 моль * 22,4 мл/ммоль = 0,9 мл
Ответ: V нер.г = 0,9 мл; m (H 2 O) = 3,2 мг
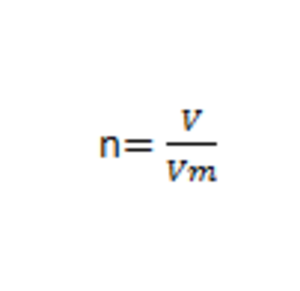
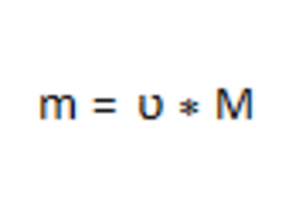
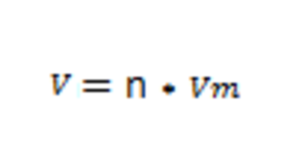
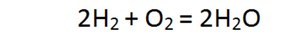
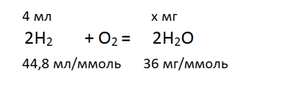
Дано:
V(O 2 ) = 3 мл
V(H 2 ) = 4 мл
Найти:
m (H 2 O) - ?
V непр.г - ?
Решение:
Уравнение реакции 4
Вычислим количество вещества кислорода и водорода по формуле: 1
n (O 2 ) = 3 мл / 22,4 мл/ммоль = 0, 13 ммоль
n (H 2 ) = 4 мл / 22,4 мл/ммоль = 0, 18 ммоль
Найдем какое вещество находится в избытке, а какое в недостатке. Определяем сколько
для реакции необходимо водорода. Слева пишем теоретические количества вещества, а
справа практические количества вещества:
2 моль (H 2 ) – х (H 2 )
1 моль (O 2 ) – 0, 13 ммоль
Находим х:
х = (2 моль * 0,13 ммоль) / 1 моль = 0,26 ммоль
Видно, что водород находится в недостатке, следовательно, считаем по водороду
количество вещества воды:
n (H 2 O) : n (H 2 ) = 1:1 из этого следует, что n (H 2 O) = n (H 2 ) = 0,18 ммоль
Вычислим массу воды по формуле: 2
М (H 2 O) = 2 * 1 + 16 = 18 мг/ммоль
m (H 2 O) = 18 мг/ммоль * 0,18 ммоль = 3,2 мг
Найдем количество вещества непрореагировавшего газа:
n неп = 0,13 ммоль – 0,09 ммоль = 0,04 ммоль
Рассчитаем объем непрореагировавшего газа по формуле: 3
V нер.г = 0,04 моль * 22,4 мл/ммоль = 0,9 мл
Ответ: V нер.г = 0,9 мл; m (H 2 O) = 3,2 мг
V(O 2 ) = 3 мл
V(H 2 ) = 4 мл
Найти:
m (H 2 O) - ?
V непр.г - ?
Решение:
Уравнение реакции 4
Вычислим количество вещества кислорода и водорода по формуле: 1
n (O 2 ) = 3 мл / 22,4 мл/ммоль = 0, 13 ммоль
n (H 2 ) = 4 мл / 22,4 мл/ммоль = 0, 18 ммоль
Найдем какое вещество находится в избытке, а какое в недостатке. Определяем сколько
для реакции необходимо водорода. Слева пишем теоретические количества вещества, а
справа практические количества вещества:
2 моль (H 2 ) – х (H 2 )
1 моль (O 2 ) – 0, 13 ммоль
Находим х:
х = (2 моль * 0,13 ммоль) / 1 моль = 0,26 ммоль
Видно, что водород находится в недостатке, следовательно, считаем по водороду
количество вещества воды:
n (H 2 O) : n (H 2 ) = 1:1 из этого следует, что n (H 2 O) = n (H 2 ) = 0,18 ммоль
Вычислим массу воды по формуле: 2
М (H 2 O) = 2 * 1 + 16 = 18 мг/ммоль
m (H 2 O) = 18 мг/ммоль * 0,18 ммоль = 3,2 мг
Найдем количество вещества непрореагировавшего газа:
n неп = 0,13 ммоль – 0,09 ммоль = 0,04 ммоль
Рассчитаем объем непрореагировавшего газа по формуле: 3
V нер.г = 0,04 моль * 22,4 мл/ммоль = 0,9 мл
Ответ: V нер.г = 0,9 мл; m (H 2 O) = 3,2 мг