Развернуть задание
Найдите массу серебра, выпавшего на стенках пробирки в виде «серебряного зеркала», при взаимодействии 140 г 10%-го раствора формальдегида с избытком аммиачного раствора оксида серебра. Рассчитайте количество вещества оксида серебра, вступившего в реакцию.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
Дано:
mр(HCOH) = 140 г
ω(HCOH) = 10%
m(Ag) - ?
ν(Ag2O) - ?
Решение:
Уравнение реакции:
mр(HCOH) = 140 г
ω(HCOH) = 10%
m(Ag) - ?
ν(Ag2O) - ?
Решение:
Уравнение реакции:
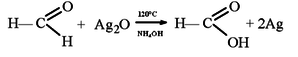
Найдем массу формальдегида, вступившего в реакцию по формулам


где ω – массовая доля вещества)
m(HCOH) = (140 г/ 100%) * 10% = 14 г
По формуле
m(HCOH) = (140 г/ 100%) * 10% = 14 г
По формуле
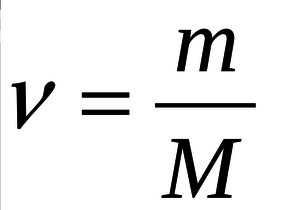
(где ν – количество вещества, m- масса вещества, M- молярная масса вещества) найдем количество вещества формальдегида
ν (HCOH) = 14 г/30 г/моль = 0,467 моль
По реакции
ν(Ag2O) = ν (HCOH) = 0,467 моль
ν(Ag) = 2 * ν (HCOH) = 0,467 моль * 2 = 0,934 моль
По формуле
ν (HCOH) = 14 г/30 г/моль = 0,467 моль
По реакции
ν(Ag2O) = ν (HCOH) = 0,467 моль
ν(Ag) = 2 * ν (HCOH) = 0,467 моль * 2 = 0,934 моль
По формуле
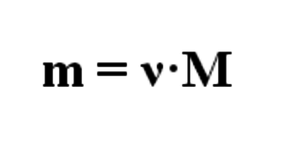
найдем массу серебра
m(Ag) = 0.934 моль * 108 г/моль = 100,87 г
Ответ: ν(Ag2O) = 0,467 моль, m(Ag) = 100,87 г
m(Ag) = 0.934 моль * 108 г/моль = 100,87 г
Ответ: ν(Ag2O) = 0,467 моль, m(Ag) = 100,87 г
Дано:
mр(HCOH) = 140 г
ω(HCOH) = 10%
m(Ag) - ?
ν(Ag2O) - ?
Решение:
Уравнение реакции:
mр(HCOH) = 140 г
ω(HCOH) = 10%
m(Ag) - ?
ν(Ag2O) - ?
Решение:
Уравнение реакции:

Найдем массу формальдегида, вступившего в реакцию по формулам


где ω – массовая доля вещества)
m(HCOH) = (140 г/ 100%) * 10% = 14 г
По формуле
m(HCOH) = (140 г/ 100%) * 10% = 14 г
По формуле
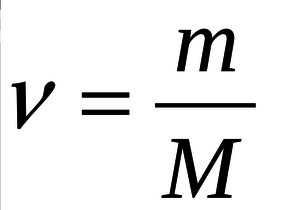
(где ν – количество вещества, m- масса вещества, M- молярная масса вещества) найдем количество вещества формальдегида
ν (HCOH) = 14 г/30 г/моль = 0,467 моль
По реакции
ν(Ag2O) = ν (HCOH) = 0,467 моль
ν(Ag) = 2 * ν (HCOH) = 0,467 моль * 2 = 0,934 моль
По формуле
ν (HCOH) = 14 г/30 г/моль = 0,467 моль
По реакции
ν(Ag2O) = ν (HCOH) = 0,467 моль
ν(Ag) = 2 * ν (HCOH) = 0,467 моль * 2 = 0,934 моль
По формуле
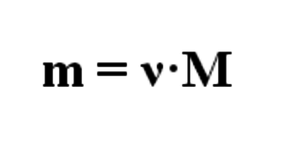
найдем массу серебра
m(Ag) = 0.934 моль * 108 г/моль = 100,87 г
Ответ: ν(Ag2O) = 0,467 моль, m(Ag) = 100,87 г
m(Ag) = 0.934 моль * 108 г/моль = 100,87 г
Ответ: ν(Ag2O) = 0,467 моль, m(Ag) = 100,87 г