Задание
Развернуть задание
Вычислить количество вещества гашеной извести, которое может быть получено из 2 т известняка, содержащего 25% примесей.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
Дано:
m(известняка) = 2 т
ω(прим.) = 25% или 0,25
n(Ca(OH)2) – ?
Решение:
1. Рассчитаем массовую долю чистого CaCO3 в известняке:
ω(CaCO3) = 100% - 25% = 75% или 0,75
2. Вычислим массу чистого CaCO3 . Так как массовая доля CaCO3 в известняке составляет 75%, то можно воспользоваться формулой:
m(известняка) = 2 т
ω(прим.) = 25% или 0,25
n(Ca(OH)2) – ?
Решение:
1. Рассчитаем массовую долю чистого CaCO3 в известняке:
ω(CaCO3) = 100% - 25% = 75% или 0,75
2. Вычислим массу чистого CaCO3 . Так как массовая доля CaCO3 в известняке составляет 75%, то можно воспользоваться формулой:
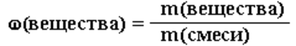
m(CaCO3) = m(известняка) ∙ ω(CaCO3) = 2 ∙ 0,75 = 1,5 т = 1,5∙10 6 г
3. Составим соотношение и найдем массу гашеной извести Ca(OH)2 :
M(CaCO3) − m(CaCO3)
M(Ca(OH)2) − m(Ca(OH)2)
M(Ca(OH)2) = 74 г/моль
M(CaCO3) = 100 г/моль
m(Ca(OH)2) = M(Ca(OH)2) ∙ m(CaCO3) / M(CaCO3) = 1,5∙10 6 ∙ 74 / 100 = 1,11∙10^6 г
4. Вычислим количество вещества по формуле:
3. Составим соотношение и найдем массу гашеной извести Ca(OH)2 :
M(CaCO3) − m(CaCO3)
M(Ca(OH)2) − m(Ca(OH)2)
M(Ca(OH)2) = 74 г/моль
M(CaCO3) = 100 г/моль
m(Ca(OH)2) = M(Ca(OH)2) ∙ m(CaCO3) / M(CaCO3) = 1,5∙10 6 ∙ 74 / 100 = 1,11∙10^6 г
4. Вычислим количество вещества по формуле:
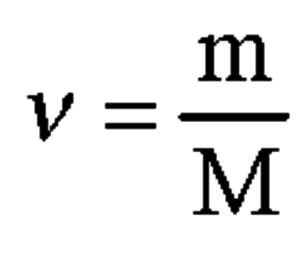
M(Ca(OH)2) = 74 г/моль
n(Ca(OH)2)= 1,11∙10^6 / 74 = 1,5∙10^4 моль = 15 кмоль.
n(Ca(OH)2)= 1,11∙10^6 / 74 = 1,5∙10^4 моль = 15 кмоль.
Дано:
m(известняка) = 2 т
ω(прим.) = 25% или 0,25
n(Ca(OH)2) – ?
Решение:
1. Рассчитаем массовую долю чистого CaCO3 в известняке:
ω(CaCO3) = 100% - 25% = 75% или 0,75
2. Вычислим массу чистого CaCO3 . Так как массовая доля CaCO3 в известняке составляет 75%, то можно воспользоваться формулой:
m(известняка) = 2 т
ω(прим.) = 25% или 0,25
n(Ca(OH)2) – ?
Решение:
1. Рассчитаем массовую долю чистого CaCO3 в известняке:
ω(CaCO3) = 100% - 25% = 75% или 0,75
2. Вычислим массу чистого CaCO3 . Так как массовая доля CaCO3 в известняке составляет 75%, то можно воспользоваться формулой:
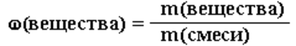
m(CaCO3) = m(известняка) ∙ ω(CaCO3) = 2 ∙ 0,75 = 1,5 т = 1,5∙10 6 г
3. Составим соотношение и найдем массу гашеной извести Ca(OH)2 :
M(CaCO3) − m(CaCO3)
M(Ca(OH)2) − m(Ca(OH)2)
M(Ca(OH)2) = 74 г/моль
M(CaCO3) = 100 г/моль
m(Ca(OH)2) = M(Ca(OH)2) ∙ m(CaCO3) / M(CaCO3) = 1,5∙10 6 ∙ 74 / 100 = 1,11∙10^6 г
4. Вычислим количество вещества по формуле:
3. Составим соотношение и найдем массу гашеной извести Ca(OH)2 :
M(CaCO3) − m(CaCO3)
M(Ca(OH)2) − m(Ca(OH)2)
M(Ca(OH)2) = 74 г/моль
M(CaCO3) = 100 г/моль
m(Ca(OH)2) = M(Ca(OH)2) ∙ m(CaCO3) / M(CaCO3) = 1,5∙10 6 ∙ 74 / 100 = 1,11∙10^6 г
4. Вычислим количество вещества по формуле:
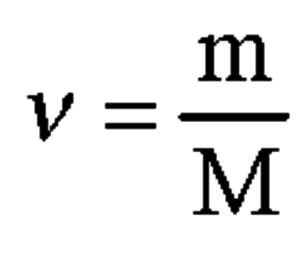
M(Ca(OH)2) = 74 г/моль
n(Ca(OH)2)= 1,11∙10^6 / 74 = 1,5∙10^4 моль = 15 кмоль.
n(Ca(OH)2)= 1,11∙10^6 / 74 = 1,5∙10^4 моль = 15 кмоль.