Задание
Развернуть задание
Составить уравнения реакций, с помощью которых можно осуществить следующие превращения:
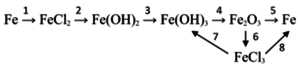
Реакции с участием электролитов записать в молекулярной и ионной форме. Рассмотреть два превращения (по выбору) с позиций окисления – восстановления.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
1) Fe + 2HCl = FeCl2 + H2↑
Fe + (2H+) + (2Cl-) = ((Fe)^(2+) +(2Cl-) + H2↑
Fe + (2H+) = ((Fe)^(2+) + H2↑
восстановитель Fe^0 – 2e → ((Fe)^(2+)) | 1 окисление
окислитель 2H+ + 2e → H2^0 | 1 восстановление
2) FeCl2 + 2NaOH = Fe(OH)2↓ + 2NaCl
(Fe^(2+)) + (2Cl-) + (2Na+) + 2OH− = Fe(OH)2↓ + (2Na+) + (2Cl−)
(Fe^(2+)) + (2OH−) = Fe(OH)2↓
3) 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3↓
восстановитель Fe^(2+) – 1e → (Fe^(3+)) | 4 окисление
окислитель O2^0 + 4e → (2O^(-2)) | 1 восстановление
4) 2Fe(OH)3 =(t) Fe2O3 + 3H2O
5) Fe2O3 + 3H2 =(t) 2Fe + 3H2O
окислитель (2Fe^(+3)) + 6e → 2Fe^0 | 1 восстановление
восстановитель H2^0 − 2e → 2H+ | 3 окисление
6) Fe2O3 + 6HCl = 2FeCl3 + 3H2O
Fe2O3 + (6H+) + (6Cl−) = (2Fe^(3+)) + (6Cl−) + 3H2O
Fe2O3 + (6H+) = (2Fe^(3+)) + 3H2O
7) FeCl3 + 3NaOH = Fe(OH)3↓ + 3NaCl
(Fe^(3+)) + (3Cl−) + (3Na+) + (3OH−) = Fe(OH)3↓ + (3Na+) + (3Cl−)
(Fe^(2+)) + (3OH−) = Fe(OH)3↓
8) 2FeCl3 + 3Zn = 3ZnCl2 + 2Fe
(2Fe^(3+)) + (6Cl−) + 3Zn = (3Zn^(2+)) + (6Cl−) + 2Fe
(2Fe^(3+)) + 3Zn = (3Zn^(2+)) + 2Fe
окислитель (Fe^(3+)) + 3e → Fe^0 | 2 восстановление
восстановитель Zn^0 − 2e → (Zn^(2+)) | 3 окисление
Fe + (2H+) + (2Cl-) = ((Fe)^(2+) +(2Cl-) + H2↑
Fe + (2H+) = ((Fe)^(2+) + H2↑
восстановитель Fe^0 – 2e → ((Fe)^(2+)) | 1 окисление
окислитель 2H+ + 2e → H2^0 | 1 восстановление
2) FeCl2 + 2NaOH = Fe(OH)2↓ + 2NaCl
(Fe^(2+)) + (2Cl-) + (2Na+) + 2OH− = Fe(OH)2↓ + (2Na+) + (2Cl−)
(Fe^(2+)) + (2OH−) = Fe(OH)2↓
3) 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3↓
восстановитель Fe^(2+) – 1e → (Fe^(3+)) | 4 окисление
окислитель O2^0 + 4e → (2O^(-2)) | 1 восстановление
4) 2Fe(OH)3 =(t) Fe2O3 + 3H2O
5) Fe2O3 + 3H2 =(t) 2Fe + 3H2O
окислитель (2Fe^(+3)) + 6e → 2Fe^0 | 1 восстановление
восстановитель H2^0 − 2e → 2H+ | 3 окисление
6) Fe2O3 + 6HCl = 2FeCl3 + 3H2O
Fe2O3 + (6H+) + (6Cl−) = (2Fe^(3+)) + (6Cl−) + 3H2O
Fe2O3 + (6H+) = (2Fe^(3+)) + 3H2O
7) FeCl3 + 3NaOH = Fe(OH)3↓ + 3NaCl
(Fe^(3+)) + (3Cl−) + (3Na+) + (3OH−) = Fe(OH)3↓ + (3Na+) + (3Cl−)
(Fe^(2+)) + (3OH−) = Fe(OH)3↓
8) 2FeCl3 + 3Zn = 3ZnCl2 + 2Fe
(2Fe^(3+)) + (6Cl−) + 3Zn = (3Zn^(2+)) + (6Cl−) + 2Fe
(2Fe^(3+)) + 3Zn = (3Zn^(2+)) + 2Fe
окислитель (Fe^(3+)) + 3e → Fe^0 | 2 восстановление
восстановитель Zn^0 − 2e → (Zn^(2+)) | 3 окисление
1) Fe + 2HCl = FeCl2 + H2↑
Fe + (2H+) + (2Cl-) = ((Fe)^(2+) +(2Cl-) + H2↑
Fe + (2H+) = ((Fe)^(2+) + H2↑
восстановитель Fe^0 – 2e → ((Fe)^(2+)) | 1 окисление
окислитель 2H+ + 2e → H2^0 | 1 восстановление
2) FeCl2 + 2NaOH = Fe(OH)2↓ + 2NaCl
(Fe^(2+)) + (2Cl-) + (2Na+) + 2OH− = Fe(OH)2↓ + (2Na+) + (2Cl−)
(Fe^(2+)) + (2OH−) = Fe(OH)2↓
3) 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3↓
восстановитель Fe^(2+) – 1e → (Fe^(3+)) | 4 окисление
окислитель O2^0 + 4e → (2O^(-2)) | 1 восстановление
4) 2Fe(OH)3 =(t) Fe2O3 + 3H2O
5) Fe2O3 + 3H2 =(t) 2Fe + 3H2O
окислитель (2Fe^(+3)) + 6e → 2Fe^0 | 1 восстановление
восстановитель H2^0 − 2e → 2H+ | 3 окисление
6) Fe2O3 + 6HCl = 2FeCl3 + 3H2O
Fe2O3 + (6H+) + (6Cl−) = (2Fe^(3+)) + (6Cl−) + 3H2O
Fe2O3 + (6H+) = (2Fe^(3+)) + 3H2O
7) FeCl3 + 3NaOH = Fe(OH)3↓ + 3NaCl
(Fe^(3+)) + (3Cl−) + (3Na+) + (3OH−) = Fe(OH)3↓ + (3Na+) + (3Cl−)
(Fe^(2+)) + (3OH−) = Fe(OH)3↓
8) 2FeCl3 + 3Zn = 3ZnCl2 + 2Fe
(2Fe^(3+)) + (6Cl−) + 3Zn = (3Zn^(2+)) + (6Cl−) + 2Fe
(2Fe^(3+)) + 3Zn = (3Zn^(2+)) + 2Fe
окислитель (Fe^(3+)) + 3e → Fe^0 | 2 восстановление
восстановитель Zn^0 − 2e → (Zn^(2+)) | 3 окисление
Fe + (2H+) + (2Cl-) = ((Fe)^(2+) +(2Cl-) + H2↑
Fe + (2H+) = ((Fe)^(2+) + H2↑
восстановитель Fe^0 – 2e → ((Fe)^(2+)) | 1 окисление
окислитель 2H+ + 2e → H2^0 | 1 восстановление
2) FeCl2 + 2NaOH = Fe(OH)2↓ + 2NaCl
(Fe^(2+)) + (2Cl-) + (2Na+) + 2OH− = Fe(OH)2↓ + (2Na+) + (2Cl−)
(Fe^(2+)) + (2OH−) = Fe(OH)2↓
3) 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3↓
восстановитель Fe^(2+) – 1e → (Fe^(3+)) | 4 окисление
окислитель O2^0 + 4e → (2O^(-2)) | 1 восстановление
4) 2Fe(OH)3 =(t) Fe2O3 + 3H2O
5) Fe2O3 + 3H2 =(t) 2Fe + 3H2O
окислитель (2Fe^(+3)) + 6e → 2Fe^0 | 1 восстановление
восстановитель H2^0 − 2e → 2H+ | 3 окисление
6) Fe2O3 + 6HCl = 2FeCl3 + 3H2O
Fe2O3 + (6H+) + (6Cl−) = (2Fe^(3+)) + (6Cl−) + 3H2O
Fe2O3 + (6H+) = (2Fe^(3+)) + 3H2O
7) FeCl3 + 3NaOH = Fe(OH)3↓ + 3NaCl
(Fe^(3+)) + (3Cl−) + (3Na+) + (3OH−) = Fe(OH)3↓ + (3Na+) + (3Cl−)
(Fe^(2+)) + (3OH−) = Fe(OH)3↓
8) 2FeCl3 + 3Zn = 3ZnCl2 + 2Fe
(2Fe^(3+)) + (6Cl−) + 3Zn = (3Zn^(2+)) + (6Cl−) + 2Fe
(2Fe^(3+)) + 3Zn = (3Zn^(2+)) + 2Fe
окислитель (Fe^(3+)) + 3e → Fe^0 | 2 восстановление
восстановитель Zn^0 − 2e → (Zn^(2+)) | 3 окисление