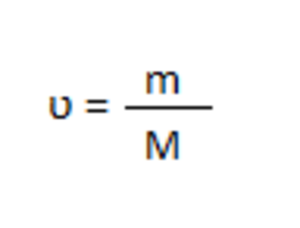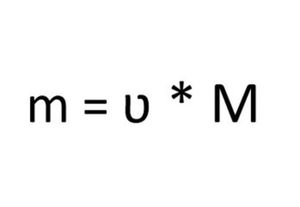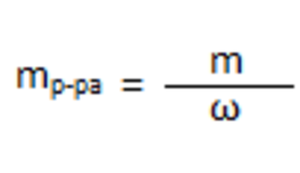Развернуть задание
Рассчитайте, сколько граммов 40%-го раствора щёлочи можно получить из 225,4 г натрия.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
Дано:
m (Na) = 225,4 г
ω (NaOH) = 40%
Найти:
m р-ра (NaOH) - ?
Решение:
2Na + 2H 2 O = 2NaOH + H 2
Рассчитаем количество вещества натрия по формуле: 1
ʋ (Na) = 225,4 г / 23 г/моль = 9,8 моль
Найдем количество вещества гидроксида натрия:
М (NaOH) = 23 + 16 + 1 = 40 г/моль
ʋ (NaOH) : ʋ (Na) = 2:2 = 1:1 из этого следует, что ʋ (NaOH) = ʋ (Na) = 9,8 моль
Рассчитаем массу гидроксида натрия по формуле: 2
m (NaOH) = 9,8 моль * 40 г/моль = 392 г
Исходя из полученных данных, найдем сколько граммов 40%-го раствора щёлочи можно
получить. Формула: 3
m р-ра (NaOH) = 392 г / 0,4 = 980 г
Ответ: m р-ра (NaOH) = 980 г
m (Na) = 225,4 г
ω (NaOH) = 40%
Найти:
m р-ра (NaOH) - ?
Решение:
2Na + 2H 2 O = 2NaOH + H 2
Рассчитаем количество вещества натрия по формуле: 1
ʋ (Na) = 225,4 г / 23 г/моль = 9,8 моль
Найдем количество вещества гидроксида натрия:
М (NaOH) = 23 + 16 + 1 = 40 г/моль
ʋ (NaOH) : ʋ (Na) = 2:2 = 1:1 из этого следует, что ʋ (NaOH) = ʋ (Na) = 9,8 моль
Рассчитаем массу гидроксида натрия по формуле: 2
m (NaOH) = 9,8 моль * 40 г/моль = 392 г
Исходя из полученных данных, найдем сколько граммов 40%-го раствора щёлочи можно
получить. Формула: 3
m р-ра (NaOH) = 392 г / 0,4 = 980 г
Ответ: m р-ра (NaOH) = 980 г
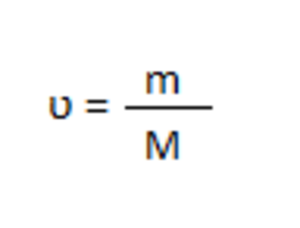
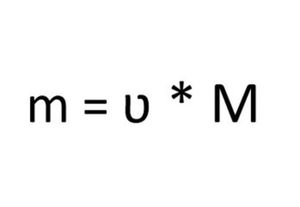
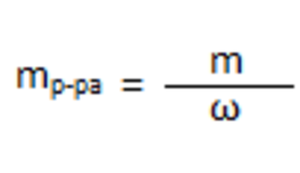
Дано:
m (Na) = 225,4 г
ω (NaOH) = 40%
Найти:
m р-ра (NaOH) - ?
Решение:
2Na + 2H 2 O = 2NaOH + H 2
Рассчитаем количество вещества натрия по формуле: 1
ʋ (Na) = 225,4 г / 23 г/моль = 9,8 моль
Найдем количество вещества гидроксида натрия:
М (NaOH) = 23 + 16 + 1 = 40 г/моль
ʋ (NaOH) : ʋ (Na) = 2:2 = 1:1 из этого следует, что ʋ (NaOH) = ʋ (Na) = 9,8 моль
Рассчитаем массу гидроксида натрия по формуле: 2
m (NaOH) = 9,8 моль * 40 г/моль = 392 г
Исходя из полученных данных, найдем сколько граммов 40%-го раствора щёлочи можно
получить. Формула: 3
m р-ра (NaOH) = 392 г / 0,4 = 980 г
Ответ: m р-ра (NaOH) = 980 г
m (Na) = 225,4 г
ω (NaOH) = 40%
Найти:
m р-ра (NaOH) - ?
Решение:
2Na + 2H 2 O = 2NaOH + H 2
Рассчитаем количество вещества натрия по формуле: 1
ʋ (Na) = 225,4 г / 23 г/моль = 9,8 моль
Найдем количество вещества гидроксида натрия:
М (NaOH) = 23 + 16 + 1 = 40 г/моль
ʋ (NaOH) : ʋ (Na) = 2:2 = 1:1 из этого следует, что ʋ (NaOH) = ʋ (Na) = 9,8 моль
Рассчитаем массу гидроксида натрия по формуле: 2
m (NaOH) = 9,8 моль * 40 г/моль = 392 г
Исходя из полученных данных, найдем сколько граммов 40%-го раствора щёлочи можно
получить. Формула: 3
m р-ра (NaOH) = 392 г / 0,4 = 980 г
Ответ: m р-ра (NaOH) = 980 г