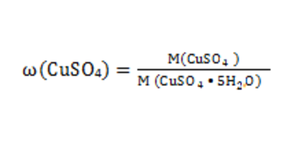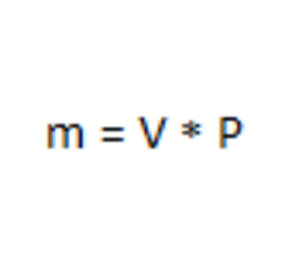Развернуть задание
В 400 мл воды растворили 40 г оксида серы (VI) (н. у.). Вычислите массовую долю серной
кислоты в полученном растворе.
кислоты в полученном растворе.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
Дано:
V (H 2 O) = 400 мл
m (SO 3 ) = 40 г
Найти:
ω (H 2 SO 4 ) - ?
Решение:
SO 3 + H 2 O = H 2 SO 4
Найдем количество вещества оксида серы (VI) и воды по формуле: 1
Переведем объем воды в массу по формуле, зная, что плотность воды равна 1 г/см 3 : 2
m (Н 2 O) = 400 мл * 1 = 400 г
Найдем молярную массу оксида серы (VI) и воды:
М (SO 3 ) = 32 + 16 * 3 = 80 г/моль
М (Н 2 O) = 2 * 1 + 16 = 18 г/моль
ʋ (Н 2 O) = 400 г / 18 г/моль =22,22 моль
ʋ (SO 3 ) = 40 г / 80 г/моль = 0,5 моль
Из расчетов мы видим, что вода находится в избытке, а оксида серы (VI) в недостатке.
Количество вещества серной кислоты считаем по недостатку, т.е. по оксиду серы (VI):
ʋ (H 2 SO 4 ) : ʋ (SO 3 ) = 1:1 из чего следует, что ʋ (H 2 SO 4 ) = ʋ (SO 3 ) = 0,5 моль
Рассчитаем молярную массу серной кислоты:
М (H 2 SO 4 ) = 2 * 1 + 32 + 16 * 4 = 98 г/моль
Найдем массу серной кислоты
m (H 2 SO 4 ) = 0,5 моль * 98 г/моль = 49 г
Масса раствора складывается из массы растворенного вещества и массы растворителя. m р-
ра =400+49г=449г
Вычислим массовую долю серной кислоты в полученном растворе по формуле 5
ω (H 2 SO 4 ) = 49 г / 449 г =0,11 или 11%
Ответ: ω (H 2 SO 4 ) = 11%
V (H 2 O) = 400 мл
m (SO 3 ) = 40 г
Найти:
ω (H 2 SO 4 ) - ?
Решение:
SO 3 + H 2 O = H 2 SO 4
Найдем количество вещества оксида серы (VI) и воды по формуле: 1
Переведем объем воды в массу по формуле, зная, что плотность воды равна 1 г/см 3 : 2
m (Н 2 O) = 400 мл * 1 = 400 г
Найдем молярную массу оксида серы (VI) и воды:
М (SO 3 ) = 32 + 16 * 3 = 80 г/моль
М (Н 2 O) = 2 * 1 + 16 = 18 г/моль
ʋ (Н 2 O) = 400 г / 18 г/моль =22,22 моль
ʋ (SO 3 ) = 40 г / 80 г/моль = 0,5 моль
Из расчетов мы видим, что вода находится в избытке, а оксида серы (VI) в недостатке.
Количество вещества серной кислоты считаем по недостатку, т.е. по оксиду серы (VI):
ʋ (H 2 SO 4 ) : ʋ (SO 3 ) = 1:1 из чего следует, что ʋ (H 2 SO 4 ) = ʋ (SO 3 ) = 0,5 моль
Рассчитаем молярную массу серной кислоты:
М (H 2 SO 4 ) = 2 * 1 + 32 + 16 * 4 = 98 г/моль
Найдем массу серной кислоты
m (H 2 SO 4 ) = 0,5 моль * 98 г/моль = 49 г
Масса раствора складывается из массы растворенного вещества и массы растворителя. m р-
ра =400+49г=449г
Вычислим массовую долю серной кислоты в полученном растворе по формуле 5
ω (H 2 SO 4 ) = 49 г / 449 г =0,11 или 11%
Ответ: ω (H 2 SO 4 ) = 11%
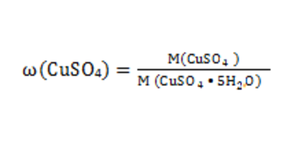

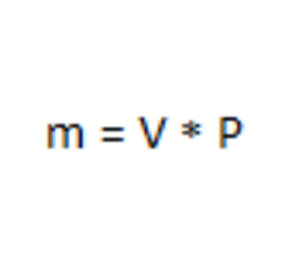
Дано:
V (H 2 O) = 400 мл
m (SO 3 ) = 40 г
Найти:
ω (H 2 SO 4 ) - ?
Решение:
SO 3 + H 2 O = H 2 SO 4
Найдем количество вещества оксида серы (VI) и воды по формуле: 1
Переведем объем воды в массу по формуле, зная, что плотность воды равна 1 г/см 3 : 2
m (Н 2 O) = 400 мл * 1 = 400 г
Найдем молярную массу оксида серы (VI) и воды:
М (SO 3 ) = 32 + 16 * 3 = 80 г/моль
М (Н 2 O) = 2 * 1 + 16 = 18 г/моль
ʋ (Н 2 O) = 400 г / 18 г/моль =22,22 моль
ʋ (SO 3 ) = 40 г / 80 г/моль = 0,5 моль
Из расчетов мы видим, что вода находится в избытке, а оксида серы (VI) в недостатке.
Количество вещества серной кислоты считаем по недостатку, т.е. по оксиду серы (VI):
ʋ (H 2 SO 4 ) : ʋ (SO 3 ) = 1:1 из чего следует, что ʋ (H 2 SO 4 ) = ʋ (SO 3 ) = 0,5 моль
Рассчитаем молярную массу серной кислоты:
М (H 2 SO 4 ) = 2 * 1 + 32 + 16 * 4 = 98 г/моль
Найдем массу серной кислоты
m (H 2 SO 4 ) = 0,5 моль * 98 г/моль = 49 г
Масса раствора складывается из массы растворенного вещества и массы растворителя. m р-
ра =400+49г=449г
Вычислим массовую долю серной кислоты в полученном растворе по формуле 5
ω (H 2 SO 4 ) = 49 г / 449 г =0,11 или 11%
Ответ: ω (H 2 SO 4 ) = 11%
V (H 2 O) = 400 мл
m (SO 3 ) = 40 г
Найти:
ω (H 2 SO 4 ) - ?
Решение:
SO 3 + H 2 O = H 2 SO 4
Найдем количество вещества оксида серы (VI) и воды по формуле: 1
Переведем объем воды в массу по формуле, зная, что плотность воды равна 1 г/см 3 : 2
m (Н 2 O) = 400 мл * 1 = 400 г
Найдем молярную массу оксида серы (VI) и воды:
М (SO 3 ) = 32 + 16 * 3 = 80 г/моль
М (Н 2 O) = 2 * 1 + 16 = 18 г/моль
ʋ (Н 2 O) = 400 г / 18 г/моль =22,22 моль
ʋ (SO 3 ) = 40 г / 80 г/моль = 0,5 моль
Из расчетов мы видим, что вода находится в избытке, а оксида серы (VI) в недостатке.
Количество вещества серной кислоты считаем по недостатку, т.е. по оксиду серы (VI):
ʋ (H 2 SO 4 ) : ʋ (SO 3 ) = 1:1 из чего следует, что ʋ (H 2 SO 4 ) = ʋ (SO 3 ) = 0,5 моль
Рассчитаем молярную массу серной кислоты:
М (H 2 SO 4 ) = 2 * 1 + 32 + 16 * 4 = 98 г/моль
Найдем массу серной кислоты
m (H 2 SO 4 ) = 0,5 моль * 98 г/моль = 49 г
Масса раствора складывается из массы растворенного вещества и массы растворителя. m р-
ра =400+49г=449г
Вычислим массовую долю серной кислоты в полученном растворе по формуле 5
ω (H 2 SO 4 ) = 49 г / 449 г =0,11 или 11%
Ответ: ω (H 2 SO 4 ) = 11%