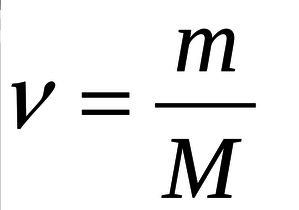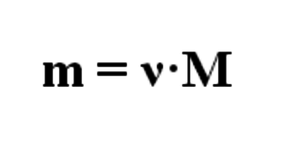Развернуть задание
Вычислите массу бромной воды с массовой долей брома 2%, которая потребуется для полного взаимодействия со 186 г 1%-го раствора анилина.
Развернуть задание
Новое решение
Решение
- Предыдущее
- Следующее
Дано:
ω(Br(2)) = 2%
m(р)(C(6)H(5)NH(2)) = 186 г
ω(C(6)H(5)NH(2)) = 1%
m(р)(Br(2)) - ?
Решение:
Из формулы на 2 картинке следует, что масса вычисляется по формуле, представленной на 3 картинке, где ω – массовая доля вещества)
m(C(6)H(5)NH(2)) = (186 г/ 100%) * 1% = 1,86 г
Найдем количество вещества анилина по формуле на 4 картинке, где ν – количество вещества, m- масса вещества, M- молярная масса вещества)
ν(C(6)H(5)NH(2)) = 1,86 г/93 г/моль = 0,02 моль
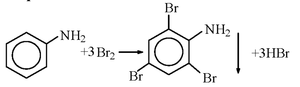
Как видно из уравнения реакции количество брома в три раза больше количества анилина
ν(Br(2)) = 3 * ν(C(6)H(5)NH(2)) = 0,06 моль
По формуле на 5 картинке найдем массу брома
m(Br(2)) = 0.06 моль * 160 г/моль = 9.6 г
Из формулы, представленной на 2 картинке, следует, что масса раствора равна (6 картинка, где ω – массовая доля вещества)
m(р)(Br(2)) = (9.6 г/ 2%) * 100% = 480 г
Ответ: 480 г
ω(Br(2)) = 2%
m(р)(C(6)H(5)NH(2)) = 186 г
ω(C(6)H(5)NH(2)) = 1%
m(р)(Br(2)) - ?
Решение:
Из формулы на 2 картинке следует, что масса вычисляется по формуле, представленной на 3 картинке, где ω – массовая доля вещества)
m(C(6)H(5)NH(2)) = (186 г/ 100%) * 1% = 1,86 г
Найдем количество вещества анилина по формуле на 4 картинке, где ν – количество вещества, m- масса вещества, M- молярная масса вещества)
ν(C(6)H(5)NH(2)) = 1,86 г/93 г/моль = 0,02 моль
Как видно из уравнения реакции количество брома в три раза больше количества анилина
ν(Br(2)) = 3 * ν(C(6)H(5)NH(2)) = 0,06 моль
По формуле на 5 картинке найдем массу брома
m(Br(2)) = 0.06 моль * 160 г/моль = 9.6 г
Из формулы, представленной на 2 картинке, следует, что масса раствора равна (6 картинка, где ω – массовая доля вещества)
m(р)(Br(2)) = (9.6 г/ 2%) * 100% = 480 г
Ответ: 480 г


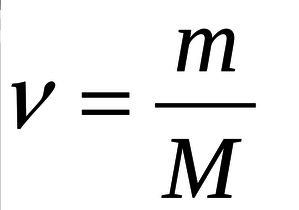
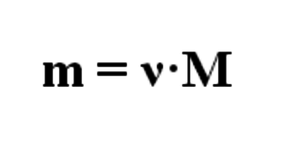

Дано:
ω(Br(2)) = 2%
m(р)(C(6)H(5)NH(2)) = 186 г
ω(C(6)H(5)NH(2)) = 1%
m(р)(Br(2)) - ?
Решение:
Из формулы на 2 картинке следует, что масса вычисляется по формуле, представленной на 3 картинке, где ω – массовая доля вещества)
m(C(6)H(5)NH(2)) = (186 г/ 100%) * 1% = 1,86 г
Найдем количество вещества анилина по формуле на 4 картинке, где ν – количество вещества, m- масса вещества, M- молярная масса вещества)
ν(C(6)H(5)NH(2)) = 1,86 г/93 г/моль = 0,02 моль
Как видно из уравнения реакции количество брома в три раза больше количества анилина
ν(Br(2)) = 3 * ν(C(6)H(5)NH(2)) = 0,06 моль
По формуле на 5 картинке найдем массу брома
m(Br(2)) = 0.06 моль * 160 г/моль = 9.6 г
Из формулы, представленной на 2 картинке, следует, что масса раствора равна (6 картинка, где ω – массовая доля вещества)
m(р)(Br(2)) = (9.6 г/ 2%) * 100% = 480 г
Ответ: 480 г
ω(Br(2)) = 2%
m(р)(C(6)H(5)NH(2)) = 186 г
ω(C(6)H(5)NH(2)) = 1%
m(р)(Br(2)) - ?
Решение:
Из формулы на 2 картинке следует, что масса вычисляется по формуле, представленной на 3 картинке, где ω – массовая доля вещества)
m(C(6)H(5)NH(2)) = (186 г/ 100%) * 1% = 1,86 г
Найдем количество вещества анилина по формуле на 4 картинке, где ν – количество вещества, m- масса вещества, M- молярная масса вещества)
ν(C(6)H(5)NH(2)) = 1,86 г/93 г/моль = 0,02 моль
Как видно из уравнения реакции количество брома в три раза больше количества анилина
ν(Br(2)) = 3 * ν(C(6)H(5)NH(2)) = 0,06 моль
По формуле на 5 картинке найдем массу брома
m(Br(2)) = 0.06 моль * 160 г/моль = 9.6 г
Из формулы, представленной на 2 картинке, следует, что масса раствора равна (6 картинка, где ω – массовая доля вещества)
m(р)(Br(2)) = (9.6 г/ 2%) * 100% = 480 г
Ответ: 480 г